REPUBLIQUE DEMOCRATIQUE DU CONGO



ECOLE DE SANTE PUBLIQUE
B.P : 1825
LUBUMBASHI


 |

 |

![]()


![]()

ECOLE DE SANTE PUBLIQUE
B.P : 1825
LUBUMBASHI




 |
 |

EPIGRAPHE
 |
Dr. Michel KASWA
DEDICACE
A mon Père
A ma mère
A mes frères
A tous mes amis et connaissances
Je vous dédie ce travail
AVANT-PROPOS
Au terme de notre premier cycle de graduat à l’école de santé publique il est d’une obligation de produire un travail scientifique dont sa réalisation n’étais pas notre affaire seule, cependant Nous rendons grâce à SEIGNEUR JESUS CHRIST, maitre des temps et des circonstances en qui nous avons la vie et l'espérance. Nous exprimons notre profonde gratitude au Pr. Dr CHENGE MUKALENGA Faustin pour la direction et plus particulièrement à Dr. CHUY KALOMBOLA Didier pour la codirection, le sacrifice et l'intérêt tout particulier accordé à ce travail si riche suite à ses orientations.
Un grand hommage mérité est rendu aux Professeurs, Chefs de Travaux et Assistants de notre Chère école pour la qualité de leurs enseignements dont nous sommes bénéficiaires.
Nous saisissons aussi cette opportunité qui nous est offerte pour remercier les membres de notre famille pour leur soutien tant financier, matériel que moral.
Nos sincères remerciements à nos parents KARUBANDIKA GULA Anaclet et RIZIKI COLLETTE et à mes frères BUKWEKWE JUSTIN GULA, DANIEL BIJA GULA, ESPOIR SALEH GULA, JEANNETTE GULA, PAPY GULA et ANACLET GULA pour leurs conseils et encouragements très riche tout au long de notre parcours académique.
A nos amis et combattants de lutte ALPHA BYADUNIA, FADHILI GLOIRE, EXAUCEE BINTI, LEVIS BUNGUKE, SUMAILI ALEXANDRE, MALEGA TRESOR, RODRICK MUTOMBO, NATHAN BOMANA, LAURENT KAPANGA, SANZU Jean-Pierre et tous les héros dans l'ombre non cités. Qu'ils trouvent ici l'expression de notre indéfectible attachement.
BIENFAIT SOBANUKA
SIGLES ET ABBREVIATIONS
ADN : Acide Désoxyribo Nucléique
BAAR : Bacille Acide alcoolorésistant
OMS : Organisation mondiale de la santé
CSDT : Centre de santé de Diagnostic et traitement
PNLT : Programme National de Lutte contre la Tuberculose
SIDA : Syndrome d’Immunodéficience Acquise
HGR : Hôpital Général de Reference
BK : Bacille de Koch
R : Rifampicine
H : isoniazide
Z : Pyraziramide
E : Etambutol
IDR : Intradermoréaction à Tuberculine
S : Streptomycine
TB : Tuberculose
TEP : Tuberculose Extra Pulmonaire
TP+ : Tuberculose Pulmonaire bacteriologiquement confirmée
TP/C : Tuberculose Pulmonaire cliniquement diagnostiquée
PATI : Programme Antituberculeux Intégré
TB-MR : Tuberculose Multirésistant
MF : Microscopie à fluorescence
VIH : Virus d’Immunodéficience Humaine
ZS : Zone de Santé
ZN : Ziehl-Neelsen
Liste annexe
Fiche d’extraction des données
Liste des tableaux
Tableau I. Répartition des cas par tranche d’âge
Tableau II. Répartition des cas par Sexe
Tableau III. Répartition des cas par Provenance
Tableau IV. Répartition des cas par Diagnostic
Tableau V. répartition des cas par localisation TEP
Tableau VI. Répartition des cas par unité de traitement
Tableau VII. Répartition des cas par co-infection TB/VIH
Liste des figures
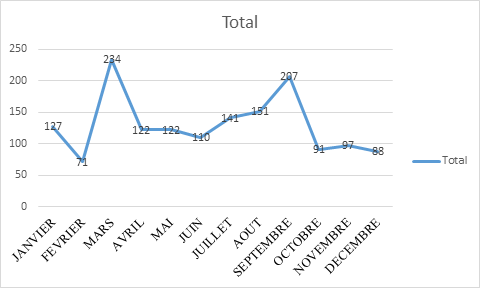
Figure 1. Répartition des cas par mois d’enregistrement
RESUME
Objectif : L'objectif de notre travail était de déterminer le profil épidémiologique des patients et les types de tuberculose chez les patients reçus à l’Hôpital général de référence, Zone de santé Kenya, ville de de Lubumbashi, République Démocratique du Congo.
Méthode : C'est une étude descriptive transversale des patients diagnostiqués et traités pour tuberculose du 1er Janvier 2019 au 31 décembre 2019 dans la zone de santé de la Kenya. Une de 11 zones de santé que compte la ville de Lubumbashi dans la province du Haut-Katanga (RD Congo). Ont été inclus tous les patients tuberculeux diagnostiqués et traités dans la zone de santé pendant la période d’étude. Les données ont été collectées par la technique dite, technique documentaire. L’âge, le sexe, la provenance, provenance, diagnostic, co-infection TB/VIH ont été les paramètres d'analyse. Les analyses ont été faites grâce aux logiciels Epi-Info et Excel
Résultat : sur un total de 260.975 habitants que compte la zone, 1561 patients tuberculeux ont étés enregistrés soit une prévalence de 0.6%. Le sexe masculin représentait 59, 39% contre 40,61% de sexe féminin avec un sexe ratio de 1.46 en faveur des hommes. La moyenne d’âge était de 33±. La majorité des patients soit 24,42% appartiennent à la tranche d’âge entre 28 et 37 ans. La tuberculose pulmonaire a représenté 71,43% contre 28.57% de tuberculose extrapulmonaire dont la localisation pleurale avait 38,56%. Avec une co-infection au VIH+ de 11,40%
Conclusion ; la tuberculose pulmonaire est une maladie fréquente avec une prévalence de 71,4% sur l'ensemble des patients reçus.
Mots-clés : Profil épidémiologique, Tuberculose, Zone de santé.
INTRODUCTION
1. ETAT DE LA QUESTION
La tuberculose est une maladie très dangereuse et contagieuse car elle occupe la neuvième cause de la mortalité dans le monde et la principale cause d’un seul agent infectieux, en tête de classement de décès par rapport au VIH/SIDA. La tuberculose touche tous les pays et toutes les tranches d’âge, mais c’est une maladie qui peut être prévenue et guérie. Elle peut toucher tout le monde, partout, mais la plupart des personnes qui développent la maladie sont des adultes, plus souvent des hommes que des femmes, et les 30 pays à forte charge de morbidité due à la tuberculose totalisent près de 90 % des cas de tuberculose survenant chaque année. La tuberculose constitue, à l’échelle mondiale, un sérieux problème de santé publique. L’Organisation mondiale de la santé (OMS) estimait ainsi qu’en 1993, un tiers de la population mondiale (soit 1,7 milliard de personnes) était infecté par le bacille de Koch (BK, Mycobacterium tuberculosis), dont, chaque année, environ 8,8 millions de personnes développeront la maladie et 3 millions mourront (OMS, 1993).
En 1996, la tuberculose fut responsable de 22,7% du nombre total des morts indigènes pour maladies infectieuses et parasitaires (2,2% des décès pour toutes les causes), c’est-à-dire deux fois le taux mondial de mortalité spécifique par tuberculose (Amarante, 1999).
L'Organisation mondiale de la santé rapporte à travers son rapport annuel consacré à la tuberculose et sorti en 2015 que 1,5 million de personnes sont mortes de la tuberculose l’année précédente. En 2016, 6,3 millions de nouveaux cas de tuberculose ont été signalés contre 6,1 millions en 2015, soit 61% de l’incidence estimée 10,4 millions. La tuberculose est l'une des principales causes de mortalité chez les personnes séropositives: en 2016, 40 % des décès dus au VIH étaient dus à cette dernière (OMS, 2016). Environ 82 % des décès dus à la tuberculose chez les personnes séronégatives se sont produits en 2016. En 2017, à l’échelle mondial 6,4 millions de nouveaux cas ont été notifiés, contre 7,0 millions en 2018 (OMS, 2019). Au total, 1,4 million de personnes sont mortes de la tuberculose en 2019 dont 208 000 présentaient également une infection à VIH dans le monde. 10 millions de personnes ont contracté la tuberculose dans le monde entier en 2019 dont, 5,6 millions d’hommes, 3,2 millions de femmes et 1,2 million d’enfants. Chez les enfants et les adolescents, la maladie n’est souvent pas reconnue par les prestataires de soins et elle peut être difficile à diagnostiquer et à traiter. Parmi les nouveaux cas de tuberculose enregistrés en 2019, 87 % sont survenus dans les 30 pays présentant la plus forte charge de la maladie (OMS, 2020).
Bien que la maladie soit curable, la forte prévalence dans les pays les plus pauvres s’explique par la conjonction d’un ensemble de facteurs : précarité, promiscuité, dénutrition, analphabétisme, infrastructure médicale insuffisante, et surtout épidémie d’infection par le VIH. La prévalence s’accroît en cas de guerre ou de famine. On constate également que l’accès au diagnostic et au traitement pose un problème dans les pays concernés. (OMS, 2020). Le risque que l’infection tuberculeuse se transforme en tuberculose évolutive est 18 (15-21) fois plus élevé chez les personnes infectées par le VIH que chez celles qui ne le sont pas. La tuberculose et le VIH forment une association meurtrière, chacun accélérant l’évolution de l’autre. En 2019, environ 208 000 personnes sont mortes d’une tuberculose associée au VIH. Le pourcentage de cas notifiés de tuberculose pour lesquels un résultat attesté de test de dépistage du VIH était disponible s’établissait à 69 % en 2019, contre 64 % en 2018 (OMS, 2020). En 2020, 198 pays et territoires représentaient plus de 99 % de la population mondiale et du nombre estimé de cas de tuberculose ont fourni des données. (OMS, 2021)
En Afrique 2016, 2,5 millions de personnes ont contracté la tuberculose, soit un quart des nouveaux cas de tuberculose dans le monde, Les enquêtes de prévalence menées de 2010 à 2016 ont révélé que, dans certains États Membres, jusqu’à la moitié des cas de tuberculose existants n’étaient pas dépistés, 417 000 personnes sont mortes de cette maladie en 2016. Plus de 25 % des décès dus à la tuberculose surviennent dans, En 2016, on estime qu'un million d'enfants ont contracté la tuberculose et que 250 000 d'entre eux en sont morts y compris les enfants atteints de tuberculose associée au VIH. (OMS Afrique, 2017). La tuberculose demeure un problème de santé majeur malgré la baisse constante et remarquable de son incidence entre 2010 et 2017, En 2017 près de 2,5 millions de nouveaux cas de tuberculose, ce qui équivaut à 25 % des cas notifiés dans le monde (OMS Afrique, 2018). Comme l’indique le rapport sur la lutte contre la tuberculose en 2018, La prévalence de la tuberculose qui était estimée à 237 cas pour 100000 habitants en 2017, était la plus forte au monde, la moyenne mondiale étant alors de 133 cas de tuberculose pour 10000 habitants. Seulement 50 % des cas de tuberculose multi-résistante sont détectés et traités convenablement. En outre, le nombre de personnes vivant avec le VIH dont le risque de contracter la tuberculose est au moins dix fois supérieur à celui des personnes séronégatives, reste très élevé. Par ailleurs, 16 des 30 pays à forte charge de tuberculose dans le monde se trouvent dans cette région et quarante-six pour cent des budgets destinés à la lutte contre la tuberculose dans les États Membres n’étaient pas financés. La tuberculose est une maladie encore largement répandue et où les mesures visant à freiner son expansion souffrent souvent de faiblesses liées aux contraintes financières, au niveau de vie de la population et au système de santé en place. (OMS Afrique, 2019). La charge de la tuberculose associée au VIH est la plus élevée, 86 % des patients atteints de tuberculose disposaient d’un résultat attesté au test de dépistage du VIH. (OMS Afrique, 2020)
La République Démocratique du Congo est parmi les trente pays de la planète les plus touchés. Il occupe le 9e rang dans le monde et le 2e en Afrique. En 2019, 180 178 malades ont été confirmés comme porteurs de la tuberculose, parmi eux, 13 878 ont été aussi coinfectés par le VIH. 92% des personnes affectées par la tuberculose et mises en traitement ont été traitées avec succès. La tuberculose constitue un problème de santé publique majeure, Notre pays est classé en Afrique en deuxième position en termes de fardeau de la tuberculose et neuvième au niveau mondial. En 2020, nous avons notifié plus de 200 000 cas de tuberculose sur l’ensemble du territoire national, il faut de moyens conséquents pour réduire le fardeau de la Tuberculose, « Chaque personne a les bacilles avec lui. Mais le bacille est dormant. Il attend des conditions favorables pour se réveiller. Et donc, chaque centimètre de ce pays est supposé couvert par les activités de lutte contre la tuberculose » (kayomo, 2020) Directeur du Programme national de lutte contre la tuberculose (PNLT), à l’occasion de la Journée mondiale de lutte contre la tuberculose, célébrée le 24 mars de chaque année par les Nations unies, La lutte contre la tuberculose est coordonnée par le programme national de lutte contre la tuberculose, Ce programme a intégré un protocole de prise en charge dans les centres de santé de dépistage et de traitement de la tuberculose (CSDT) réunissant théoriquement un équipement minimum pour répondre aux besoins de la population dans cette matière. En passant de 180.000 cas de tuberculose en 2019 à plus de 202.145cas en 2020 constitue une raison de plus pour s’inquiéter (Kayomo, 2021). La tuberculose est une maladie infectieuse d’origine bactérienne potentiellement grave qui touche principalement les poumons, l’année dernière (2020), en dépit de la survenue de la maladie à covid-19, pour la première fois, nous avons dépassé la barre de 200000cas de tuberculose notifiés en une seule année (E. Longondo, 2021). Au niveau de la coordination Provinciale de lutte contre la tuberculose Katanga Sud, l'incidence de la tuberculose est estimée à 0.18% pour une population estimée à 3 636 747 habitants en 2010 et le taux de décès chez les nouveaux cas de tuberculose à microscopie positive a été estimé à 5% pour 3687 cas enregistrés au cours de la même année. Au cours de 2011 la Zone de santé de Lubumbashi a rapporté 708cas de tuberculose sur une population de 134 804 habitants soit une prévalence de 0,5%. (Tshamba, 2014). La propagation de la tuberculose est plus favorisée par des facteurs tels que la promiscuité qui est très manifesté surtout en milieu urbain congolais. Peu d’étude ont cependant porté sur le profil épidémiologique de la tuberculose dans les villes congolaises telles que Lubumbashi, c’est pourquoi notre étude consistera à combler les vides en ce qui concerne la connaissance de cette maladie par la population lushoise tout en contribuant à lutter contre la tuberculose.
2. PROBLEMATIQUE ET HYPOTHSES DE RECHERCHE
Sur une population mondiale estimable en 2020 de 7,7millliards, voir la tuberculose elle-même rapporter plus de 10millions de nouveaux cas, c’est vraiment une question préoccupante (OMS, 2020). Chaque individu a les bacilles avec lui. Mais le bacille est dormant, il attend des conditions favorables pour se réveiller. Et donc, chaque centimètre de ce pays est supposé couvert par les activités de lutte contre la tuberculose (Kayomo, 2021).
La tuberculose touche principalement les adultes pendant les années les plus productives de leur vie, mais le risque existe pour toutes les tranches d’âge. Parmi les sujets infectés par le bacille tuberculeux, le risque de développer la maladie à un moment quelconque de la vie se situe entre 5 % et 15 %. Ce risque est toutefois beaucoup plus élevé chez les personnes qui ont un système immunitaire déficient, notamment celles qui vivent avec le VIH ou qui souffrent de malnutrition ou de diabète, ainsi que chez les consommateurs de tabac (OMS, 2020). Le présent travail vise à répondre à la quête principale de savoir : Quel est le profil épidémiologique (Incidence, Prévalence et facteurs de risques), de la tuberculose dans la zone de santé de la Kenya ?
3. OBJECTIFS DU TRAVAIL
Objectif général
Ce travail a pour objectif, de contribuer à la lutte contre la tuberculose dans la zone de sante de la Kenya.
Objectifs spécifique
Les objectifs spécifiques de notre travail sont :
- Déterminer l’incidence et la prévalence de la tuberculose dans la zone de sante de la Kenya
- Identifier les caractéristiques sociodémographiques et cliniques de la tuberculose au sein la zone de santé Kenya
4. CHOIX ET INTERET DU SUJET
Nous avons porté notre choix sur ce sujet, en vue de son importance dans la population Congolaise toute entière et plus précisément celle de la Zone de santé de Kenya, car nous trouvons qu’il est vraiment nécessaire que cette dernière change de perspective sur cette maladie autre fois considérée comme tant d’autres.
Notre étude comprend trois volets d’intérêt.
Intérêt personnel : Ce sujet nous permettra d’approfondir les connaissances sur la tuberculose partant de nos recherches que nous aurions à faire tout au long de ce travail.
Intérêt scientifique : Le présent travail avec comme sujet, profil épidémiologique de la tuberculose dans la zone de sante de la Kenya, constitue un support de référence utile pour les chercheurs qui voudront avoir une connaissance dans ce domaine.
Intérêt social : Ce travail aidera la population Lushoise à bien observer les mesures des préventions de la tuberculose en vue d’éviter la survenue de cette dernière.
5. DELIMITATION SPACIO-TEMPOREL DU TRAVAIL
Dans l’espace notre recherche sera limitée dans la zone de santé de Kenya car elle constitue notre lieu d’étude.
Dans le temps, la recherche s’étendra de l’année 2O19-2020 ce choix porté sur cet intervalle nous permettra de faire une comparaison entre les années antérieures et une année postérieure.
6. SUBDIVISION DU TRAVAIL
Le présent travail est subdivisé en deux grandes parties excepté l’introduction et la conclusion. La première partie de considérations théoriques comprend deux chapitres. Le chapitre premier traite de manière générale la tuberculose. La deuxième partie, expose le cadre empirique. Il comporte trois chapitres. Le chapitre deuxième présente les matériels et méthodes. Le chapitre troisième présente les résultats. Le chapitre quatrième, discute sur les résultats.
PREMIERE PARTIE : CONSIDERATIONS THEORIQUES
CHAPITRE I. LA TUBERCULOSE
Il s’agit d’une maladie à évolution et dissémination lentes dans les sociétés humaines. Elle se distingue des autres maladies contagieuses (grippe ou rougeole, par exemple) par divers aspects. Sa période d’incubation est de durée variable, parfois de plusieurs années. Elle est également silencieuse sur le plan clinique. Bien que sa période de contagiosité soit plus longue (quelques semaines à quelques mois, voire plusieurs années), elle est peu contagieuse. Contrairement à la rougeole ou autrefois à la variole, par exemple, qui infectent une population entière lors d’une première exposition à leur virus, on estime qu’un individu porteur d’une tuberculose pulmonaire peut infecter dix personnes par an dans des conditions naturelles, c’est-à-dire en l’absence de traitement (Styblo, 1980).
La tuberculose est une maladie infecto-contagieuse due à une mycobactérie (le bacille de Koch) qui se transmet par voie aérienne d’une personne malade à un individu sain. En parlant, chantant, éternuant ou toussant, le malade projette dans l’air de fines gouttelettes de salive infectées. Le risque de transmission est lié à la densité de bacilles dans l’air inspiré mais aussi à la fréquence, à la durée et à l’intensité des contacts avec un individu contagieux [Sudre, 1993] La tuberculose est une maladie infectieuse causée par la bactérie Mycobacterium tuberculosis, contagieuse, avec des signes cliniques variables. Elle arrive en tête des causes de mortalité d'origine infectieuse à l’échelle mondiale, devant le sida. L'Organisation mondiale de la santé rapporte à travers son dernier rapport annuel consacré à la tuberculose et sorti en 2015 que 1,5 million de personnes sont mortes de la tuberculose l’année précédente (OMS, 2016).
I.1 HISTOIRE DE LA TUBERCULOSE
Maladie au long cours aux manifestations très diverses et affectant aussi bien humains et animaux, la tuberculose est une maladie très ancienne, mais dont l'unité nosologique et l'étiologie ne furent établies qu'au XIXe siècle. Une ancienne théorie du XXe siècle postulait que la tuberculose humaine à M. tuberculosis dérivait de la tuberculose bovine à M. bovis, en étant une conséquence de la domestication animale. Les études génomiques indiquent que M. tuberculosis et bovis ont évolué à partir d'un ancêtre commun présent chez les mammifères et qui aurait infecté les hominidés d'Afrique de l'est, il y a trois millions d'années. Cet ancêtre commun aurait Co-évolué avec ses hôtes pour aboutir aux mycobactéries humaines et animales actuelles. Les souches modernes pathogènes M. tuberculosis seraient issues d'un clone apparu il y a 15 000 à 20 000 ans, ou 11 000 ans, à partir d'une souche ancestrale de M. tuberculosis. (Ousamma, 2015) Dès l’Antiquité gréco-romaine, plusieurs auteurs ont décrit une maladie amaigrissante au long cours, dénommée suivant les uns « phtisie » (pour dépérissement), suivant les autres « tabès ». Hippocrate (Ve – IVe siècle av. J.-C.) puis Galien (IIe siècle apr. J.-C.) et Caelius Aurelianus (Ve siècle) en ont dressé les symptômes, notamment pulmonaires. Arrêtée de Cappadoce (fin du IIe siècle) en a cependant dressé la description la plus détaillée. Ces descriptions initiales n’ont guère subi de modifications notables jusqu’au début du XIXe siècle. L'origine de la maladie a été débattue durant l'Antiquité, entre héréditaire ou contagieuse, plus tard, Avicenne décrira la tuberculose comme uniquement contagieuse. (Berche, 2007) C'est en 1733 que Pierre Desault, chirurgien à Bordeaux, fait paraître un Essai sur la phtisie où il affirme notamment que la lésion fondamentale de la phtisie est le tubercule, et est encore un des premiers à signaler la parenté entre la phtisie pulmonaire et les formes ganglionnaires. L'invention du stéthoscope par René Laennec en 1817 facilite le diagnostic de la maladie. En 1839, le médecin allemand Johann Lukas Schönlein rassemble en une description unifiée les manifestations cliniques disparates de la maladie. Jusqu'alors, « phtisie » et « tuberculose » étaient souvent considérées comme deux entités, voisines mais distinctes. Si Schönlein forge en 1834 le terme de tuberculose, composé d'un nom latin et d'une terminaison grecque, la littérature médicale, tout comme le langage commun, continuera d'utiliser indistinctement, jusqu'au début du XXe siècle, les termes de « phtisie », « consomption » et « tuberculose ». (Codell, 2010)
De 1865 à 1868, le médecin Jean-Antoine Villemin reproduit chez les animaux (lapins, cobayes) les lésions de la tuberculose humaine, par inoculation de tissu altéré humain. Il peut ainsi affirmer que cette maladie, de nature jusqu'alors inconnue, est due à un microbe invisible par les moyens techniques de l'époque. Il démontra en 1869 que la transmission se fait par voie aérienne. Ses conclusions se heurtent à une forte opposition, en France notamment. Elles inspirent cependant des travaux comme ceux d'Edwin Klebs, Julius Cohnheim, Carl Salomonsen et Tappeiner qui aboutissent à établir de façon indubitable la contagiosité de la maladie (Regan, Morisky, 2010) ;
En 1882 enfin, à la suite des travaux de Louis Pasteur, Robert Koch met en évidence le bacille tuberculeux à partir de lésions humaines : le 24 mars 1882, il communique d'abord à la Société de Physiologie de Berlin une note sur la recherche et la culture du bacille de la tuberculose ; le 10 avril, il publie dans le Berliner klinische Wochenschrift un mémoire sur l'étiologie de la tuberculose qu'il rapporte à un bacille décelé dans les crachats et les lésions tuberculeuses humaines.(Svetlana, 2020)
I.2 SYMPTOMES DE LA TUBERCULOSE
Fièvre légère ; Toux persistante ; Expectorations (crachats) de couleur inhabituelle ou sanguinolentes; Perte d’appétit et de poids ; Sueurs nocturnes ; Douleurs dans la poitrine à la respiration ou pendant la toux ; Douleurs à la colonne vertébrale ou aux articulations. (J. Allard, 2013)
I.3 FORMES DE TUBERCULOSE
La tuberculose peut revêtir différentes formes selon la localisation du foyer infectieux. Sa manifestation clinique la plus fréquente est la forme pulmonaire (la phtisie selon Hippocrate). C’est elle qui est principalement responsable de la transmission des BK. Les symptômes de la tuberculose pulmonaire sont bien connus. Certains sont assez évocateurs, telles la toux prolongée (de plus de trois semaines), l’expectoration ou encore l’hémoptysie. Fatigue et faiblesse sont aussi des plaintes communes. Le malade peut également présenter amaigrissement, perte de l’appétit, fièvre nocturne de faible intensité, douleur thoracique, transpiration nocturne et tremblements (Gentilini, 1993).
On distingue 3 formes de tuberculose.
La tuberculose pulmonaire ou phtisie : C’est la forme la plus courante de tuberculose (environ 70 % des cas). Les bactéries détruisent les tissus pulmonaires, créant ainsi des cavités. La maladie reste localisée dans les poumons ;
La tuberculose extra pulmonaire : Dans ce cas, les bactéries attaquent d’autres parties du corps, comme les os, les reins, les ganglions lymphatiques, les méninges ou le système nerveux central. La tuberculose extra pulmonaire s’accompagne ou non d’une tuberculose pulmonaire ;
La tuberculose disséminée ou miliaire : (comme des graines de millet disséminées dans tout le poumon, lui donnant une apparence caractéristique). Les bactéries se répandent par le système sanguin et attaquent l’ensemble de l’organisme. Il s'agit donc d'une tuberculose pulmonaire et extra pulmonaire. (Passeport santé, 2011)
I.4 TYPES DE TUBERCULOSE
I.4.1 La tuberculose ganglionnaire
Elle est très fréquente au même titre que la tuberculose pulmonaire. Les adénopathies sont souvent médiatisnales et hilaires. Elles sont en général de taille modérée, mais peuvent parfois obstruer une bronche. En périphérie les adénopathies sont surtout cervicales, puis axillaires et inguinales. Initialement fermes et mobiles, les ganglions sont ensuite fixés par une péri-adénite avec peu de signes inflammatoires. Les fistules externes à bord irrégulier laissent ensuite sourdre (suinter) un pus caséeux qui se recouvre de croûtes. C'est cette maladie, nommée scrofule ou écrouelles que les rois de France et d'Angleterre étaient censés guérir par simple toucher. La croyance et les cérémonies qui y étaient attachées ont perduré jusqu'au XIXe siècle. Le diagnostic repose sur l’examen bactériologique du liquide de ponction et l’examen anatomopathologique à la suite de la biopsie ganglionnaire. L’apparition des signes généraux doivent encourager un traitement sans attendre le diagnostic microbiologique dans ces pays. Selon la même étude faite en Tunisie (une région endémique de la tuberculose) qui a porté sur cinquante patients atteints de la tuberculose ganglionnaire, il a été remarqué que les adénopathies étaient principalement cervicales (75 %), puis médiastinales (21 %), sus-claviculaires (9,4 %) et axillaires (6,3 %). Les tailles ont été retrouvées surtout entre 3 et 5 cm. Les adénopathies étaient inflammatoires ou fermes. Dans 21,9 % des cas, la tuberculose ganglionnaire était associée à d’autres types de tuberculose. La bactériologie a permis le diagnostic chez 65,6 % des cas. (Marrakchi, Maaloul, 2010)
I.4.2 Tuberculose urogénitale
La tuberculose urogénitale est responsable de 14 à 41 % des atteintes extra pulmonaires. Le rein est très souvent infecté lors d’une tuberculose miliaire le plus souvent au niveau du cortex rénal. Cliniquement, les lésions sont très souvent unilatérales. Au niveau du rein, elles sont préférentiellement situées dans la médullaire où elles vont produire des granulomes épithélioïdes avec une nécrose caséeuse (lésion spécifique à la tuberculose) aboutissant à une destruction tissulaire (Watfa et Frederic, 2005). L’atteinte se manifeste par des symptômes liés à la distension rénale en cas d’atteinte urétérale. Elle peut se manifester cliniquement par une cystite banale. Or, le diagnostic est évoqué devant une pyurie sans germe. En cas de lésion génitale, les lésions touchent fréquemment l’épididyme se traduisant par une épididymite. Environ 50 à 75 % des hommes avec une atteinte génitale ont des anomalies radiologiques au niveau de l’appareil urinaire (W. Saeed, 2012) Un bilan radiologique de tout l’appareil urinaire (uroscanner) est toujours indiqué ainsi qu’une radiographie du thorax à la recherche d’une localisation pulmonaire. Le clinicien oriente vers l’examen cytobactériologique des urines afin de confirmer son diagnostic. (L. Wang et al, 2003)
I.4.3 Tuberculose ostéoarticulaire
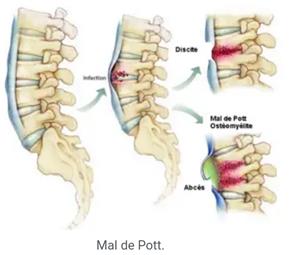 |
La forme la plus fréquente et la plus redoutable est la tuberculose rachidienne dite mal de Pott ; La localisation au niveau de l’espace intervertébral (mal de Pott) est la plus fréquente des localisations ostéoarticulaires et la plus grave car elle siège au voisinage des structures nerveuses importantes. Elle représente 10 % des cas de tuberculose (L. Boussel, B. Marchand, 2002). Selon la même étude faite en Tunisie (une région endémique de la tuberculose) qui a porté sur cinquante patients atteints de la tuberculose ganglionnaire, il a été remarqué que les adénopathies étaient principalement cervicales (75 %), puis médiastinales (21 %), sus-claviculaires (9,4 %) et axillaires (6,3 %). Les tailles ont été retrouvées surtout entre 3 et 5 cm. Les adénopathies étaient inflammatoires ou fermes. Dans 21,9 % des cas, la tuberculose ganglionnaire était associée à d’autres types de tuberculose. La bactériologie a permis le diagnostic chez 65,6 % des cas (Marrakchi, Maaloul, 2010).
I.4.4 Méningite tuberculeuse
Une forme extrêmement rare, mais très redoutable. Le tableau clinique et radiologique est atypique. Elle touche les enfants et les adultes jeunes. Dans sa forme typique la méningite tuberculeuse associe un syndrome méningé et un syndrome infectieux progressif et peu intense : fièvre au long cours, otalgie, vomissement. À la suite de la pratique de la PL, le LCR est classiquement clair, avec une lymphocytose, une hyperalbuminorachie et une hypoglucorachie. Sa gravité nécessite la mise en route rapide du traitement. Des séquelles fonctionnelles s’observent dans plus d’un tiers des cas : hémiplégie, paralysie des paires crâniennes, troubles sensoriels, calcifications intracrâniennes, etc. (S. Hafaied, Hamdi, 2015)
I.4.5 Tuberculose cutané
Rare en Occident où elle ne représente que 1,5 à 2,1 % de l'ensemble des formes que peut prendre la tuberculose, la forme cutanée de la tuberculose est cependant endémique en région tropicale et au Maghreb (H. Lakhdar 2005). Elle adopte alors des formes cliniques variées : chancre tuberculeux, tuberculose cutanée miliaire, lupus tuberculeux, scrofulodermes ou gommes tuberculeuses, ou encore tuberculose péri-orificielle (Beyt, Ortbalds, 1980). La classification de Beyt de 1980, basée sur des critères physiopathologiques, est aujourd'hui la référence pour distinguer les diverses formes : tuberculose d’inoculation (source exogène) : chancre tuberculeux, tuberculose verruqueuse, certains lupus vulgaris ; tuberculose secondaire (source endogène) : scrofuloderme (par contiguïté); tuberculose orificielle (auto-inoculation) ;tuberculose hématogène : certains lupus vulgaris, tuberculose miliaire aiguë, gomme tuberculeuse ; tuberculose éruptive (tuberculides) : lichen scrofulosorum, tuberculose papulonécrotiques, érythème induré de Bazin, vascularite nodulaire (Tigoulet, Fournier, 2001)
I.5 CONTAGION DE LA TUBERCULOSE
La primo-infection tuberculeuse, consécutive à l’inhalation du BK et à son implantation dans les alvéoles pulmonaires, est généralement asymptomatique, la personne infectée n’étant pas contagieuse. Dans 90% des cas, les défenses immunitaires de l’individu sont suffisantes pour empêcher la multiplication et la dispersion des BK dans son corps, ce qui se traduit par une réaction tuberculinique positive. Dans 10% des cas, l’infection devient patente. C’est la tuberculose-maladie ou tuberculose primaire : on considère généralement que 5% des personnes infectées développeront la maladie dans les deux ans qui suivent l’infection, les 5% restants à n’importe quel moment de leur vie (Sudre, 1993).
La primo-infection regroupe les manifestations cliniques, radiologiques et bactériologiques, survenant après un premier contact infectant avec le bacille de Koch. Elle est souvent asymptomatique chez l’adulte mais la littérature rapporte qu’elle peut être symptomatique chez les enfants à 90 % associant les signes généraux ; les symptômes sont dominés par la toux chez plus de la moitié des cas, les douleurs thoraciques chez 20 % des cas, et la dyspnée (L. Jeannin, 1997). L’examen clinique met en évidence des adénopathies périphériques chez 37,5 % et la confirmation du diagnostic se fait à travers l’intradermoréaction à tuberculine (IDR).
Le dépistage de la tuberculose pulmonaire se fait généralement au cours de consultation habituelle par un interrogatoire auprès des malades qui présentent principalement des signes d’imprégnation ainsi que des symptômes respiratoires persistant pendant plus de deux semaines (Fikal, Sajiai, 2016).
Cependant, le tableau symptomatique peut être polymorphe, représentatif dans son ensemble de toute la séméiologie broncho-pulmonaire.
Symptômes et signes clinique de la tuberculose
|
Symptômes |
Primo infection |
TBC pulmonaire |
|
Toux |
|
+++ |
|
Fatigue/malaise |
+ |
++ |
|
Perte pondérale |
+ |
++ |
|
Sudations nocturnes |
|
++ |
|
Hémoptysies |
|
+ |
|
Douleurs thoracique |
+ |
+ |
|
Signes Clinique |
|
|
|
Fièvre |
+ |
++ |
|
Râles à l’auscultation |
|
+ |
+++ = courant (> 50 %), ++ occasionnel, + rare
Le diagnostic repose sur les différents éléments allant de l’interrogatoire à l’examen physique et clinique. L’interrogatoire doit enquêter sur la notion de contagion en tenant compte de la physiopathologie de la maladie et les modalités du développement de la lésion. L’installation de la maladie peut se faire progressivement en s’étalant sur plusieurs semaines et l’examen clinique se révèle utile à la recherche des éléments d’orientation vers l’affirmation du diagnostic (L. Jeannin, 1997). Quant à l’examen clinique, les éléments qui peuvent faire suspecter la TBC sont nombreux : Signe généraux : signes d’imprégnation tuberculeuse, fébricule, sueurs nocturnes et aménorrhée chez la femme. Signes fonctionnels apparents au début de l’affection et sont durables à plus de 15 jours. Ils sont marqués principalement par les signes suivants : toux productive, expectoration purulente, dyspnée. L’examen physique relève à son tour à travers l’auscultation et la palpation de la poitrine des râles crépitant mais il se peut qu’il s’avère neutre et sans particularité (Brandlia et al, 2003). En revanche quand il s’agit d’une installation brutale, l’hémoptysie et crachats sanguins sont plus observés chez les personnes atteintes ainsi que l’épanchement pleural est observé que ce soit aérien ou liquidien (A.Tazi, 1998). Le clinicien devant un contexte de symptomatologie pulmonaire qui persiste au-delà de 15 jours, et en tenant également compte de la prévalence dans la région en cause, est en mesure de suspecter la tuberculose et procède à la procédure de l’affirmation de diagnostic. Cela doit conduire vers des examens complémentaires : radiographie du thorax et l’examen cytobactériologique des crachats (Hochedez, Zeller, 2003). Le diagnostic définitif est fondé sur l’isolement ou la culture du bacille, habituellement à partir des crachats. Les cavernes sont une complication fréquente de la tuberculose pulmonaire (Catherine, Paul, 2014). On appelle caverne une cavité creusée au sein du parenchyme pulmonaire. Les bacilles tuberculeux se développent initialement dans le poumon sous forme de nodules, appelés granulomes, qui sont peu à peu entourés de lymphocytes et de macrophages destinés à contenir l'infection. Un granulome peut évoluer soit vers la disparition sans cicatrice, soit vers la caverne, sans que les mécanismes sous-jacents soient compris en totalité. Les vestiges de macrophages détruits occupent le centre du granulome et forment la majeure partie de la nécrose caséeuse (keertan, Helen, 2005). Chez certains patients, cette nécrose caséeuse se liquéfie et devient un milieu de culture adapté aux bacilles, qui prolifèrent. Des enzymes protéolytiques érodent alors la capsule fibreuse située en périphérie du granulome, et son centre liquide peut alors se vider peu à peu (keertan, Helen, 2005). Lorsqu'une caverne tuberculeuse arrive en communication avec l'arbre bronchique, la dissémination des bacilles dans l'air expiré augmente la contagiosité. Par ailleurs, la quantité importante de bacilles contenus dans les cavernes favorise le développement de résistances aux anti-tuberculeux (W.Saeed, 2012).
La primo-infection peut évoluer de trois façons
· La guérison complète après un stade exsudatif plus ou moins aigu, avec présence d’assez nombreux bacilles et polynucléaires
· Formation de tubercules (stade prolifératif), guérison lente par fibrose et finalement calcification (lésions pauci bacillaires)
· Évolution par extension et confluence des tubercules, la liquéfaction du caséum crée une cavité ; si celle-ci s’ouvre dans une bronche, il y a apport d’oxygène nécessaire au bacille qui est aérobie, et la lésion devient pluri bacillaire (un million de bacilles dans une caverne de 2cm). Cette évolution défavorable se produit dans environ 5% des cas
Quelques faits relatifs à la transmission de la tuberculose :
Le bacille de Koch se transmet par des gouttelettes de salive qui se retrouvent en suspension dans l’air lorsqu’une personne tousse, éternue, chante ou joue d’un instrument à vent, et non en touchant une personne contagieuse ; Il faut généralement un contact répété ou prolongé avec une personne contagieuse pour contracter l’infection ;Seules les personnes qui présentent des symptômes sont contagieuses; une personne contagieuse qui suit un traitement médicamenteux n’est plus contagieuse après deux ou trois semaines de traitement.(J. Allard, 2013)
I.6 PERSONNES A RISQUE DE LA TUBERCULOSE
La tuberculose touche principalement les adultes pendant les années les plus productives de leur vie, mais le risque existe pour toutes les tranches d’âge. Plus de 95 % des cas et des décès concernent les pays en développement. Le risque de développer une tuberculose évolutive est 18 fois plus élevé parmi les personnes infectées par le VIH. Les sujets atteints d’autres affections affaiblissant le système immunitaire présentent également un risque accru de tuberculose évolutive. Chez les personnes souffrant de dénutrition, le risque est trois fois plus élevé que la normale. En 2019, 2,2 millions de nouveaux cas de tuberculose étaient imputables à la dénutrition dans le monde.
Les troubles liés à la consommation d’alcool et le tabagisme augmentent le risque d’apparition de la maladie d’un facteur 3,3 et 1,6, respectivement. Parmi les nouveaux cas de tuberculose survenus dans le monde en 2019, 0,72 million étaient imputables à des troubles liés à la consommation d’alcool et 0,70 million au tabagisme. (OMS, 2020)
I.7 FACTEURS DE RISQUE DE LA TUBERCULOSE
La maladie comprend deux étapes : la tuberculose-infection qui peut rester latente et silencieuse, puis la tuberculose-maladie où les troubles se manifestent. Le risque de contracter une tuberculose dépend d'abord du risque d'exposition au bacille (infection), puis du risque de développer la maladie après infection.
1. Un premier facteur de risque est le contact étroit avec un cas contagieux ; la promiscuité respiratoire (familles nombreuses sous un même toit, personnes ayant vécu ou vivant dans des pays de forte endémie tuberculeuse, conditions de logement, populations pénitentiaires, etc.) est généralement en cause.
2. Un second risque est lié à l'état de santé du sujet infecté : malnutrition (carence en protéines), enfant de moins de cinq ans, personnes âgées, diabétique (Thanh, 2015), personnes en situation de déficience immunitaire (par infection VIH ou sous traitement immunosuppresseur, etc. (D. Che, 2012).
3. Enfin la promiscuité et la pauvreté sont deux facteurs historiques connus : au cours du XVIIIe siècle, près d'une personne sur quatre était atteinte de tuberculose en occident. L'épidémie atteint son apogée au XIXe siècle au cours duquel près de dix millions de personnes sont victimes de la tuberculose. Environ un tiers des décès enregistrés aux États-Unis et en Europe sont causés par cette « peste blanche » (S. Henry, 2013).
La révolution industrielle provoque en effet une augmentation de la population et, conséquemment une recrudescence des maladies contagieuses. De plus, les conditions de travail du XIXe siècle européen, qui subsistent encore dans plusieurs pays, ont été et sont des facteurs aggravants : les travaux pénibles, de longues journées de travail, des ateliers surpeuplés, l'atmosphère empoussiérée (poussières textiles, métalliques, minérales, organiques, etc.), ainsi que les conditions de logements (promiscuité, manque d'air et de soleil, maisons « meurtrières »), la malnutrition, le tabagisme et les mauvaises mœurs (crachats, saleté, manquement aux règles d'hygiène corporelle) (Flurin, Worboys, 2010) ; tous ces facteurs peuvent se combiner pour favoriser ou aggraver l'infection tuberculeuse.
La tuberculose est un indicateur de la précarité sociale, et du niveau des systèmes de santé (dépistage, diagnostic et soin). (D. Che, 2012)
4. Le diabète semble être un facteur favorisant : alors que cette maladie est en voie de « pandémisation » dans les pays riches notamment, mais de plus en plus aussi dans les pays émergents et pauvres où d'après l’OMS en 2013, plus de 80 % des 3,4 millions de décès annuels par diabète sont survenus. Des études trouvent une incidence de tuberculose deux à huit fois plus élevée chez le diabétique par rapport à la population moyenne (Banyai1993), (Stevenson, 2007), (Jeon, 2008) ce qui ferait du diabète un facteur de risque. En outre, le diabète modifie la présentation clinique de la tuberculose (âge d’apparition et poids corporel plus élevés) ; il pourrait modifier la réponse aux médicaments antituberculeux (temps de « négativation » bactériologique plus long) et il pourrait aggraver la transmission et la mortalité par tuberculose (Alisjahbana, Sahiratmadja, 2007).
5. Le fait de vivre en Asie est un facteur prédisposant : la plupart des nouveaux cas (49 %) se situent dans les zones peuplées d'Asie : Bangladesh, Pakistan, Inde, Chine et Indonésie. Il existe une augmentation dans les pays de l'Europe de l'Est dont la Russie (Christopher Dye, 2006) ou l'Ukraine. La croissance reste très forte en Afrique, avec près de 13 % contre moins de 1 % dans les pays asiatiques.
6. Prise de drogues : l'injection par voie intraveineuse et surtout chez les porteurs du virus de l'immunodéficience humaine (VIH), aggrave son incidence, qui atteint ici 12,5 %, soit environ 1,2 million de personnes en 2014 (P. Benkimoun, 2016)
Cette infection touche l'adulte jeune, et les hommes sont près de deux fois plus atteints que les femmes. La malnutrition et les intoxications médicamenteuses sont des causes reconnues de l'augmentation du nombre de cas.
I.8 MESURES PREVENTIVES DE BASE DE LA TUBERCULOSE
Respecter les mesures d’hygiène. Pour les personnes qui sont souvent en relation avec des tuberculeux : lavage des mains fréquent, port d’un masque au besoin. Prendre soin de sa santé. Avoir une alimentation saine et équilibrée, dormir suffisamment, faire de l’exercice physique régulièrement, éviter d’être en situation de stress chronique, etc. Cela offre les meilleures chances d’avoir un système immunitaire vigoureux. Pour en savoir davantage, consulter notre fiche Renforcer son système immunitaire et notre section Vivre en santé. Détecter et traiter une infection latente. Les personnes qui travaillent dans des milieux à risque ou qui ont été en contact prolongé avec un malade en phase active peuvent subir un test cutané afin de déceler la présence de la bactérie dans le corps (voir la description du test dans la section Traitements médicaux). Si le résultat est positif, un traitement préventif aux antibiotiques permet généralement d’éviter que la maladie se déclenche. Ce traitement préventif est plus simple et nécessite l’utilisation de moins de médicaments que pour traiter une tuberculose active. S’informer auprès de son médecin ou des autorités compétentes de son lieu de travail. (J. Allard 2013).
I.8 DIAGNOSTIC DE LA TUBERCULOSE
Diagnostic bactériologique, après avoir extrait des expectorations ou du liquide de ponction auprès du malade, l’échantillon du prélèvement fait l’objet d’un examen cytobactériologique à travers les différentes techniques (Brandlia, 2003) : coloration de Ziehl-Neelsen (ZN) : La méthode de ZN, datant de 1880 est la méthode la plus fréquemment utilisée. C’est un examen rapide, simple, et très spécifique (> 95 % dans les pays à haute prévalence). Elle permet de mettre en évidence le caractère Acid alcoolorésistant des bactéries. L'observation et l’identification des bactéries s'effectuent à l’aide du microscope optique, avec objectif à immersion. Les mycobactéries apparaissent alors comme des bacilles rouges sur fond bleu-gris (Bonnet 2011). Microscopie à fluorescence (MF) : après coloration à l’auramine elle augmente de 10% la sensibilité de la détection au microscope par rapport à la méthode classique de ZN, cet examen reposant sur le microscope à fluorescence, n’est pas utilisé dans tous les laboratoires au pays de sud en raison de son cout élevé. Examen de culture : C’est l’examen de référence des TBC utilisant traditionnellement un milieu solide Löwenstein-Jensen riche en protéines et ressources énergétiques nécessaires à la prolifération de la bactérie (L.Kivihya, 2003). En comparaison avec la méthode classique sur milieu solide, l’utilisation des milieux liquides augmente la sensibilité de plus de 10 % tout en réduisant le délai de la culture de six à deux semaines. Les performances se révèlent excellentes avec une sensibilité de 99 % et une spécificité de 100 %. (Maugein et Bébéar, 2003). La spécificité des modalités de diagnostic a fait l’objet de plusieurs études d’évaluation d’efficacité. Une étude rapporte que la méthode de coloration Z de N et la MF bénéficient d’une spécificité élevée allant jusqu’à 98 % dans le cas de la MF. Une étude montre également que la concordance diagnostique entre la MF et la culture (souvent prise comme référence) est largement supérieure à celle qui existe entre la méthode de ZN et la culture (95,1 % contre 69,6 %) (Bonnet, 2011). Les méthodes de ZN et l’examen de culture apportent une grande valeur diagnostique vue leur caractère économique en termes de cout. Ils sont des examens peu couteux et accessibles et fortement recommandés dans le diagnostic de la TBC. Ils se révèlent très pratiques et efficaces dans le diagnostic des tuberculoses ganglionnaire, pulmonaire, méningée et ostéoarticulaire. (Maugein et Bébéar, 2003)
Diagnostic anatomopathologique, l’examen anatomopathologique se pratique sur l’échantillon résultant de la biopsie. Il met en évidence une lésion spécifique à la tuberculose dite : granulome épitheloide gigantocellulaire à centre caséeux nécrosé. Le terme de granulome désigne l’ensemble des éléments cellulaires présents dans un foyer inflammatoire. Le foyer tuberculeux est entouré d’une grande cellule polynucléaire résultant de la fusion des macrophages tel que mentionné dans la physiopathologie de la maladie. (P.Hochedez, 2003)
Diagnostic moléculaire, met en évidence la présence de l’ADN du germe dans l’échantillon issu de la ponction ou des crachats en cas de TBC pulmonaire. La technique de l’art et telle que recommandée par l’OMS est réalisée à l’aide d’un dispositif nommé GeneXpert et l’utilisation du test rapide Xpert MTB/RIF. La technique s’appuie sur l’amplification de l’ADN germique via la cartouche Xpert MTB/RIF riche en ADN polymérase (enzyme intervenant dans la réplication de l’ADN au cours du cycle cellulaire) et les ressources énergétiques et protéiques nécessaires à cette procédure. Son utilisation a largement augmenté depuis 2010, date à laquelle l’OMS a recommandé pour la première fois son utilisation (D. Alland, 2015). Cela comporte un avantage majeur portant sur son efficacité et son faible coût. De nombreuses études ont évalué l’efficacité de la cartouche dans la mise en évidence des BK et BK résistants à la Rifampicine ; il est rapporté par une méta-analyse compilant plusieurs études que le test MTB/RIF est spécifique à plus de 90 % et présente un outil important facilitant l’accès à un diagnostic précis à faible cout. La mise en évidence des BK est établie dans 2 heures après le test. (M. Bates, 2016) Diagnostic radiologique, la modalité de diagnostic radiologique se révèle très utile et indiquée comme étant un examen de première intention en cas de tuberculose pulmonaire et ostéoarticulaire. Cela est justifié par les images radiologiques plus ou moins spécifiques à la tuberculose. La littérature rapporte que la spécificité varie de 27 à 81 % selon l’étude. Les imageries idéales et révélatrices de la tuberculose répondent à certains attributs dont le premier est lié au siège. En raison de l’affinité que les BK ont envers les régions aérées, la lésion radiologique est souvent observée dans les parties hautes des poumons. Néanmoins, l’image radiographique peut contenir différentes formes : infiltrat : traduisant des lésions débutantes de l’infection via une opacité peu dense, hétérogène et étendue ; nodule: granulome de taille variable, isolé ou groupé ; tuberculome : nodule isolé pseudo tumoral ; caverne : excavation par perte de substance au sein d’un infiltrat, aux parois épaisses. (J. Andreu, 2005)
Types de patients diagnostiqués
Tuberculose bactériologiquement confirmée : Sera défini comme cas de tuberculose bactériologiquement confirmé (TB+) : tout malade présentant au moins 1 frottis positif sur 2 échantillons quelle que soit sa sérologie VIH ; Tout cas avec crachat positif au TDR Xpert : MTB présent (very low, low, medium, high) ou MDRTB plus (Hain test) sans résistance à la Rifampicine. Tout patient produisant un échantillon dont la culture est positive. Les cas de tuberculose pulmonaire bactériologique ment confirmés sont les plus nombreux.
Tuberculose cliniquement diagnostiquée (TB/C) : Il s’agit des cas de tuberculose dont la présence des bacilles n'est pas prouvée (décision du clinicien tenant compte de l'histologie de la radiographie, etc. Les critères d’orientation seront les mêmes que pour la tuberculose bactériologiquement confirmée, mais la preuve bactériologique manque : Excepté les cas de miliaire aiguë pulmonaire (avec symptômes et radiographie typique), le traitement des cas présumés de tuberculose pulmonaire à frottis négatif peut être différé pour une période de surveillance de 7 jours permettant de répéter les examens microscopiques de crachats (jusqu’à 2 séries de 2 frottis Ziehl ou Auramine) à coupler avec l’avis médical pour le tuberculeux avec test VIH négatif ; Tandis que le cas présumé tuberculeux pulmonaire à microscopie négative mais avec test VIH positif ne devra pas être gardé plus d’une semaine sans traitement spécifique. Pendant cette période d’attente, le patient sera sous antibiothérapie à large spectre durant au moins 5 jours. Il peut s’agir d’une forte présomption à la radiographie pulmonaire sans résultats par la culture ou TDR. Mais dès qu’un de ces examens est positif, les malades sera reclassé dans le groupe des bactériologiquement confirmé ; Si seul les résultats des frottis à la recherche des BAAR sont disponibles et qu’ils négatifs alors on notera TP0 ou TP-. Dans le cas où l’examen de TDR est facilement accessible, il peut être utilisé en test de diagnostic initial chez les malades présumés tuberculeux VIH+ positifs Les figures 1 et 2 schématisent le résumé de la démarche diagnostique pour le présumé tuberculeux et le sujet contact.
I.9 TRAITEMENT DE LA TUBERCULOSE
En 1894, Carlo Forlanini met au point la première méthode thérapeutique invasive avec le pneumothorax artificiel intrapleural : par une injection d'air dans la cavité thoracique, entraînant la rétraction du poumon infecté, il obtient une amélioration de la maladie. En 1940, Selman Waksman découvre l'action antituberculeuse de l'actinomycine puis, en 1942, de la streptothricine. Ces antibiotiques ne peuvent toutefois être utilisés en thérapeutique humaine ou vétérinaire du fait de leur trop grande toxicité. En 1943, Waksman découvre enfin la streptomycine qui permet, un an plus tard, la première guérison par antibiotique d'un malade gravement atteint de tuberculose (M. Lubin, 2010). En 1948, a lieu le premier essai clinique randomisé de l'histoire de la médecine : l'épidémiologiste Austin Bradford Hill montre que la streptomycineest plus efficace que la collapsothérapie (R. Doll, 1998)
Le traitement est d'une durée de six mois pour une tuberculose pulmonaire à bacille de Koch sensible chez un patient immunocompétent, comprenant 2 mois de quadrithérapie antibiotique (isoniazide, rifampicine, pyrazinamide et éthambutol), puis 4 mois de bithérapie (isoniazide et rifampicine). Le traitement prolongé est indispensable afin de guérir la maladie et éviter l'émergence de souches résistantes dont l'évolution est souvent beaucoup plus grave.La rifadine est un traitement qui peut être utilisé pour traiter la tuberculose osseuse. L'isoniazide est utilisé généralement à la dose de 5 mg, en association avec trois autres antibiotiques. L’isoniazide inhibe la multiplication des bactéries responsables de la tuberculose. Ce médicament doit être administré à jeun. Antibiorésistance : une large épidémie de cas de tuberculose résistante à ce médicament s'est déclarée à Londres de 1995 à 2006 (HAS, 2016). La rifampicine est utilisée habituellement à la dose de 10 mg/kg et par jour, pendant une durée de six mois, pour le traitement de la tuberculose. Cet antibiotique est un fort inducteur enzymatique : il accélère la dégradation des autres médicaments, notamment les contraceptifs oraux. Les femmes sous contraceptifs sont donc invitées à revoir leur traitement à la hausse (après consultation du gynécologue), voire à passer à une contraception mécanique (préservatif…) pendant la durée du traitement. La rifampicine provoque une coloration orangée des urines. C'est un bon moyen d'objectiver l'observance du traitement. La streptomycine (découverte par Selman Waksman vers 1946) fut le premier antibiotique actif contre le bacille de Koch. Il est contre-indiqué chez la femme enceinte et doit impérativement être associé à d'autres antituberculeux (INH et PAS). Par voie intramusculaire chez l'adulte : 15 à 25 mg/kg et par jour. Par voie intrarachidienne : pour l'adulte, 25 à 100 mg/j, pour un enfant, 20 à 40 mg/kg et par jour en deux ou quatre injections. Surveillance du traitement : les fonctions auditives et rénales devront être surveillées régulièrement. L'éthambutol est utilisable chez la femme enceinte. Elle doit être utilisée le matin à jeun en une seule prise, quinze à vingt milligrammes par kilogramme. Ne pas dépasser vingt-cinq milligrammes par kilogramme par 24 heures sans dépasser soixante jours, puis réduire à quinze milligrammes par kilogramme et par jour. Surveillance par un fond d'œil et un examen de la vision des couleurs mensuels. Le bédaquiline (R207910), une molécule de la famille des diarylquinolines, pourrait se révéler prometteuse contre Mycobacterium tuberculosis. Elle fait naître trois espoirs : raccourcissement de la durée du traitement ; envisager des prises une seule fois par semaine en association avec un autre antituberculeux ; être active sur des souches multi résistantes, avec une efficacité bactéricide bien supérieure à celle de l'isoniazide et de la rifampicine. Ce médicament est actuellement en phase très précoce de son développement. Seules des études approfondies chez l'humain permettront de vérifier que ces espoirs sont fondés. Des corticoïdes sont ajoutés au traitement antituberculeux en cas de méningite tuberculeuse, de résistances ou de rechute de traitement. La corticothérapie doit être commencée après instauration de l'antibiothérapie, à la dose de 0,5 à 1 mg/kg et par jour pour une durée d’un à deux mois. (H. Maguire, 2006).
Les antibiotiques de première ligne peuvent vaincre la tuberculose dans presque tous les cas. On demande aux personnes atteintes de rester chez elles ou de porter un masque en public jusqu’à ce que le médecin détermine qu’elles ne sont plus contagieuses (habituellement, après deux ou trois semaines de traitement). Traitement de première ligne. On prescrit généralement les quatre antibiotiques suivants : l’isoniazide, le rifampine, l’éthambutol et le pyrazinamide, qui sont administrés par voie orale. Pour être efficace et tuer complètement les bactéries, le traitement médical exige de prendre les médicaments quotidiennement sur une période minimale de 6 mois, parfois jusqu’à 12 mois. Tous ces antibiotiques peuvent causer des dommages au foie à différents degrés. Il faut donc aviser son médecin si certains symptômes se manifestent, tels des nausées et vomissements, une perte d'appétit, une jaunisse (un teint jaunâtre), des urines foncées ou une fièvre sans cause apparente
Traitements de seconde ligne. Si les bactéries sont résistantes aux deux principaux antibiotiques (isoniazide et rifampine), on parle alors de multi-résistance (TB-MR) et il faut recourir aux médicaments de 2e ligne. On combine parfois de 4 à 6 antibiotiques. Ils doivent souvent être pris sur une plus longue période, parfois jusqu’à 2 ans. Ils peuvent aussi provoquer des effets indésirables, par exemple, des engourdissements dans les mains ou les pieds, et une toxicité du foie. Certains d’entre eux sont administrés par intraveineuse. (J. Allard, 2013)
La tuberculose est une maladie que l’on peut traiter et guérir. Les patients atteints de tuberculose évolutive pharmaco sensible suivent un traitement standard de 6 mois associant 4 médicaments antimicrobiens et reçoivent des informations et un soutien de la part d’un agent de santé ou d’un volontaire qualifié. Sans ce soutien, il est plus difficile pour les patients d’adhérer au traitement. Le diagnostic et le traitement de la tuberculose ont permis de sauver plus ou moins 63 millions de vies depuis 2000 (OMS, 2020).
I.10 CO-INFECTION TB/VIH
La Tuberculose et le VIH sont deux maladies qui s’influencent mutuellement et qui s’accompagnent d’un lourd fardeau socioéconomique pour les populations du monde en général et de la RDC en particulier. En effet, la tuberculose est la principale cause de décès observés chez les PVVIH. L’infection à VIH a un effet amplificateur sur la tuberculose. D’une part, la TB liée au VIH est évitable et guérissable, et ses effets néfastes sur le VIH peuvent donc être limités ; d’autre part, le traitement antirétroviral (TAR) prévient la TB et réduit le risque d’apparition d’une TB évolutive.
I.10.1 Dépistage Systématique du VIH chez les Tuberculeux
Pour arriver au dépistage du VIH, le personnel soignant les tuberculeux doit assurer systématiquement des services de conseil et dépistage à visée diagnostic du VIH à tous les tuberculeux. Il doit convaincre le malade tuberculeux de faire les tests de dépistage au VIH dans un délai acceptable, qui n’excèdera pas un mois. Les services de conseil et de dépistage du VIH seront offerts de manière systématique aux patients tuberculeux dans les structures sanitaires. Le conseil inclut les points suivants :
1. L’explication du lien entre le VIH et la TB ; 2. L’explication de la signification des différents résultats du test ; 3. L’explication des possibilités de prise en charge qui existent. Pour ce faire, le prestataire aura à suivre les étapes suivantes :
- Informer le caractère volontaire et confidentiel du service avec le patient tuberculeux ; - Obtenir le consentement éclairé du patient tuberculeux ; - Informer sur les différents résultats du test de dépistage VIH ; - Ne donner les résultats du test préférentiellement qu’à la personne concernée ; - Assurer le suivi psychologique du patient tuberculeux ; - Assurer la référence si nécessaire vers les structures de prise en charge appropriée ; - Prendre en charge le patient co-infecté.
I.11 TUBERCULOSE PHARMACORESISTANTE
Une résistance aux médicaments antituberculeux selon que les antécédents thérapeutiques seront définie comme une résistance primaire ou acquise.
La résistance primaire est la présence d’une souche résistance à un ou plusieurs antituberculeux chez un nouveau patient tuberculeux n’ayant jamais reçu de médicaments antituberculeux auparavant.
La résistance acquise est celle rencontrée chez un patient déjà traité, comme conséquence d’un traitement mal prescrit ou mal appliqué.
Cas résistant : Cas de tuberculose qui présente des bacilles résistants à un ou plusieurs antituberculeux de première intention.
Monorésistance : Résistance à un seul antituberculeux de première intention Poly résistance : Résistance à plus d`un antituberculeux de première intention autre que la Rifampicine et l’Isoniazide.
Multirésistance (TB-MR) : Résistance à au moins la Rifampicine et l’Isoniazide Ultrarésistance (TB-XDR) : Résistance à une fluoroquinolone et à au moins un des trois médicaments injectables de deuxième intention (amikacine, capréomycine et kanamycine), en plus de la multirésistance.
Résistance à la rifampicine : résistance à la rifampicine : détectée au moyen de méthodes phénotypiques ou génotypiques, avec ou sans résistance aux autres antituberculeux
La prise en charge des cas de TB pharmacorésistante fait partie de la stratégie « Halte à la Tuberculose » dans sa 2ème composante et aussi est restée un des axes prioritaires dans le 1er pilier de la stratégie End TB. L’un des objectifs prioritaires du PNLT est de prévenir la survenue de la tuberculose multi résistante par la prise supervisée des médicaments à des doses correctes et pendant une durée précise.
DEUXIEME PARTIE : CADRE EMPIRIQUE
CHAPITRE II. MATERIELLES ET METHODES
II.1 TYPE D’ETUDE
En ce qui concerne notre travail, nous avons mené une étude d’observation descriptive transversale.
II.2 MILIEU D’ETUDE II.2.1 La ville de Lubumbashi
Fondée en 1910 par les Belges sous le nom d'Élisabethville, la ville fut renommée Lubumbashi en 1966. Elle fut aussi la capitale de l'éphémère État autoproclamé du Katanga (1960-1963), né sous l'impulsion de Moïse Tshombe. Elle se trouve en République démocratique du Congo et chef-lieu de la province du haut-Katanga avec une population estimable à 2 988 170hab. et une superficie de 747Km² et elle est la deuxième ville de la RDC.
Le Maire de la ville : Guylain Lubaba Buluma Altitude : 1 230 m Latitude : entre 11° 20′ et 12° Sud Longitude : entre 27° 10′ et 27° 40′ Est Climat : tropical à deux saisons : sèche : d'avril à octobre pluvieuse : novembre à mars avec une pluviométrie moyenne de 1 228 mm d'eau Températures : moyenne : 20 °C les plus basses : 15,8 °C en moyenne, mais pouvant descendre jusqu'à 10 °C au mois de juillet; les plus hautes : 22,5 °C en moyenne pouvant monter à 38 °C en octobre.
Elle est divisée en sept communes dont une rurale :
Commune Annexe (rurale) Kamalondo Kampemba Katuba Kenya Lubumbashi Rwashi
II.2.2 Historique de la zone de santé Kenya
La zone de santé Kenya est une entité urbano – rurale. Elle a actuellement une population élevée à 260.975 habitants sur une superficie de 25 Km2. Elle s’étend sur la totalité de la commune de Kenya et sur une partie de la commune Annexe.
Son historique est étroitement lié à celui de l’HGR Kenya. Ce dernier fut construit vers les années 1954-1955 afin d’accueillir les malades de tuberculose dont la prévalence était très élevée dans cette partie de la ville de Lubumbashi, alors Elisabethville. La politique coloniale Belge de l’époque dans le secteur de la santé visait l’éradication de certaines maladies dont la tuberculose, cette pathologie qui ravageait la population autochtone. Il est cependant important de retenir qu’à cette époque, seuls les soins octroyés à la population comptaient, et l’organisation administrative en tant que zone de santé était inexistante.
Au fil des années, le centre de dépistage de la tuberculose prit la forme d’une formation hospitalière ou d’autres services venaient l’élargir le paquet minimum d’activités autrefois limité au dépistage de la TBC. Le souci d’organiser administrativement le ministère national de la santé poussa le gouvernement à mettre sur pieds les structures de représentation au niveau tant national, provincial, urbain que local. C’est dans cet ordre d’idées qu’est née d’abord la zone de santé Kenya – Kamalondo, devenue avec le dernier aménagement, zone de santé Kenya. Elle a en son sein un HGR et d’autres structures sanitaires disséminées sur son étendue. Elle est actuellement constituée de dix – huit aires de santé dont dix dans la partie urbaine et trois dans la partie rurale.
La zone de santé Kenya est dirigée par un Médecin Chef de Zone de Santé (MCZS) qui est entouré des autres membres de l’Equipe Cadre de la Zone de Santé (ECZS)
II.2.3 Situation géographique
La zone de sante Kenya est limitée :
- Au Nord par la zone de santé Mumbunda avec laquelle elle est séparé par le Boulevard Katuba,
- Au Nord – Est par la zone de santé Kamalondo avec laquelle elle est séparée par le rail allant aux usines GECAMINES de Lubumbashi,
- À l’Est par la zone de Santé Kampemba avec laquelle est séparée par le rail allant vers Sakania
- Au Sud – Est par la zone de santé Kisanga avec laquelle elle est séparée par la rivière Kasungami
- À l’Ouest par la zone de santé Katuba avec laquelle est séparée par la rivière Lubumbashi.
II.3 Unité d'analyse
Les structure dans lesquelles nous avions mené notre étude sont l'hôpital général de référence de la Kenya qui est une structure de deuxième échelon et fournissant le paquet complémentaire d'activité et qui est encore un (CSDT) et le Centre de santé Kenya I, structure de premier échelon et fournissant le PMA qui est en soit un (CST).
II.4 Population d'étude
Notre travail avait pour population d’étude, l'ensemble de tuberculeux traités dans la Zone de santé Kenya.
II.5 Échantillonnage
- Technique
Nous avions procédé par l’échantillonnage non-probabiliste
- Critère d’inclusion et d’exclusion
Sont inclus dans notre étude tous les tuberculeux traités dans la zone de santé de Kenya pendant la période d’étude (Du 1er janvier 2019 au 31decembre 2019) et sont exclus dans notre étude les tuberculeux non traités dans la zone de santé de Kenya.
- Taille : Nous avions considéré 1561 patients de la tuberculose dans la zone de santé Kenya
II.6 Collecte des données
Nature : Notre collecte s’est basée sur les informations sociodémographiques et Cliniques de patients tuberculeux.
Sources: nos données ont été trouvées dans les Registres des malades
Technique de collecte: la technique dont nous avions opté pour la collecte des données est la technique documentaire.
Outil de collecte : l'outil qui nous a permis à récolter les données est la fiche d'extraction
Mode de collecte : nous avions eu les renseignements sur le tuberculeux en faisant des captures de photos dans les registres
II.7 Analyse des données
Pour analyser les variables nous avions procédé par :
- Dépouillement et classification par structure - Encodage par masque de saisie - Traitement : pour traiter les données nous avions fait recours au logiciel d'analyse statistique Epi-info et Microsoft Excel
Nous avons calculé la prévalence de la tuberculose de la manière suivante : 1561*100/260975 = 0,6%
II.8 Aspects Éthiques
La conduite de l'étude a été approuvée par le MCZ de la Kenya. Etant donné que dans toute recherche, des règles éthiques et déontologiques sont à respecter. De ce fait lors de notre recherche, le consentement libre et éclairé a été respectées et pour garantir la confidentialité, les données obtenues ont été récolté et traité dans l’anonymat
II.9 Difficultés rencontrées
Lors de notre étape de collecte des données nous avions connu quelques contraintes pour atteindre notre objectif, mais une seule a attiré notre attention :
- Difficultés d’accéder aux registres des tuberculeux suite à la grève et là on était obligé de payer quelques choses pour y accéder malgré l’approbation du MCZ de la Kenya
CHAPITRE III. PRESENTATION DES RESULTATS
III.1 Caractéristiques de patients inclus dans cette étude Tableau I. Répartition par tranche d’âge
|
Tranche |
Fréquence |
Pourcentage |
|
>1 – 10 |
63 |
4,04% |
|
>10 – 19 |
159 |
10,19% |
|
>19 – 28 |
358 |
22,95% |
|
>28 – 37 |
381 |
24,42% |
|
>37 – 46 |
295 |
18,91% |
|
>46 – 55 |
170 |
10,90% |
|
>55 – 64 |
73 |
4,68% |
|
>64 – 73 |
47 |
3,01% |
|
>73 – 80 |
7 |
0,45% |
|
>80 |
7 |
0,45% |
|
Total |
1561 |
100,00% |
Ce tableau nous montre que la majorité des patients soit 24,42% appartiennent dans la tranche d’âge entre 28 et 37 ans. La moyenne d’âge était de 33ans.
|
Sexe |
Fréquence |
Pourcentage |
|
F |
634 |
40,61% |
|
M |
927 |
59,39% |
|
Total |
1561 |
100,00% |
Tableau II. Répartition par sexe
Ce tableau nous renseigne que les patients de sexe masculin étaient plus touché avec 59,39% soit 927 cas contre 40,61% soit 634 cas avec un sexe ratio de 1,46 pour les hommes.
Tableau III. Répartition par provenance
|
PROVENANCE |
Fréquence |
Pourcentage |
|
HORS ZONE |
1106 |
70,85% |
|
ZONE |
455 |
29,15% |
|
Total |
1561 |
100,00% |
La majeure partie des sujets concernés par notre étude venaient Hors Zone soit 70,85% contre 29,15% qui venaient de la Zone.
III.2 Fréquences de la tuberculose chez les patients considérés dans cette étude
Tableau IV. Répartition par diagnostic
|
DIAGNOSTIC |
Fréquence |
Pourcentage |
|
TEP |
446 |
28,57% |
|
TP/C |
212 |
13,58% |
|
TP+ |
903 |
57,85% |
|
Total |
1561 |
100,00 |
Les résultats nous montrent que la tuberculose pulmonaire a été la plus représenté avec 71,43% dont 57,85% pour le la tuberculose pulmonaire bactériologiquement diagnostiqué (TP+) et 13,58% pour la tuberculose pulmonaire cliniquement confirmé (TP/C) contre 28,57% de cas la tuberculose extra pulmonaire(TEP).
|
LOCALISATION |
Fréquence |
pourcentage |
|
Abdominale |
70 |
15,70% |
|
Ganglionnaire |
78 |
17,49% |
|
Méningée |
5 |
1,12% |
|
Osseuse |
121 |
27,13% |
|
Pleurale |
172 |
38,56% |
|
Total |
446 |
100,00% |
Tableau V. Répartition de la TBC par localisation
Les données de 446 patients nous montrent qu’il y avait plus autant la TEP Pleural avec 172 cas soit 38,56% et la localisation la moins représentée est la TEP méningée avec 5cas soit 1,12%.
Tableau VI. Répartition par co-infection TB/VIH
|
COINFECTION |
Fréquence |
Pourcentage |
|
NON |
1383 |
88,60% |
|
OUI |
178 |
11,40% |
|
Total |
1561 |
100,00% |
Le ci-haut nous montre que 1383 cas qui occupent 88,60% de notre taille n’étaient pas Co-infecté contre 178 qui représentent 11,40% étaient Co-infecté
Tableau VII. Répartition des patients unité de traitement
|
UNITE |
Fréquence |
Pourcentage |
|
CS |
65 |
4,16% |
|
HGR |
1496 |
95,84% |
|
Total |
1561 |
100,00% |
La majeure partie de patients soit 1496 cas qui représentent 95,84% ont été pris en charge par l’hôpital général de référence contre 65cas soit 4 ,16% qui ont été prise en charge par le centre de santé.
Cette figure nous montre que la courbe est ascendante au mois de mars avec 234 cas qui représentent 14,99%. Ce qui ressort que la saison sèche domine avec 51,4% contre 48,6% pour la saison pluvieuse.
|
|
Figure 1. Répartition des patients par mois d’enregistrement
CHAPITRE IV. DISCUSSION DES RESULTATS
Notre étude revêt un intérêt particulier en ce sens qu'elle permet de nous donner un aperçu sur le fonctionnement des centres de santé de dépistage et de traitement de la Zone de Santé de la Kenya. Elle a porté sur 1561 cas de tuberculose enregistré dans ces centres de dépistage et de traitement.
Au cours de la période d’étude, une prévalence de 455 cas de tuberculose pour 100 000 habitants a été notée dans la Zone de Santé de la Kenya. Cette prévalence semble confirmer la position de la République Démocratique du Congo où celle-ci est placée dans la zone à 300 et plus de cas pour 100 000 habitants (M.Muteya, 2014) et est sensiblement supérieure aux constats observés par d'autres auteurs (Mitiraoui et Al. 2014), (Brudey, 2006). Ceci serait le reflet probable de la gravité de la maladie dans notre zone de santé mais ce taux élevé pourrait être lié à une amélioration du dispositif de surveillance.
Dans notre étude, les hommes (59,39%) sont plus affectés que les femmes (40,61%). Nos résultats sont presque identiques à ceux d'autres études (Muteya, 2014. Baroux, 2010). Les patients tuberculeux enregistrés dans les CSDT de la Zone de Santé de la Kenya avaient un âge moyen de 33 ans ± et les tranches d’âge les plus atteintes étaient celles de 28-37 ans (24.42%) et 19-28 ans (22.59%).Ces résultats se rapprochent de ceux de (Mtiraoui et al. 2014) qui ont fait au cours d'une étude effectuée dans la région sanitaire de Sousse en Tunisie.
Le protocole national de prise en charge de la tuberculose recommande que les CSDT couvrent toute la juridiction de la zone de santé pour une facilité d'accès. Les CSDT de la Zone de Santé de la Kenya ont été fréquentés par les habitants venant de toute la ville de Lubumbashi mais la fréquentation des habitants provenant de la Zone de santé Kenya (29,15%) a été plus importante.
La forme clinique de la tuberculose est dominée par la localisation Pulmonaire (71.43%) et la forme clinique des tuberculoses extrapulmonaires la plus fréquente est l'atteinte pleurale (38,56%). Bien que, l'atteinte pleurale soit la forme la plus fréquente des atteintes extrapulmonaires de la tuberculose, comme l'ont aussi constaté (Baroux et D'Ortenzio, 2010) dans leurs études faites dans l’île de la Réunion « notre constat par rapport à la forme clinique la plus fréquente diffère de celui obtenu dans la région sanitaire de Sousse, en France et l’île de la Réunion où la forme pulmonaire est la plus fréquente dans les proportions respectives de 66%, 71.1% et 81% ».
CONCLUSION
Cette étude sur la tuberculose dans la zone de santé de la Kenya, nous a permis de noter que la sur un total de 260.975 habitants que compte la zone, 1561 patients tuberculeux ont étés enregistrés soit une prévalence de 0.6%. Le sexe masculin représentait 59, 39% contre 40,61% de sexe féminin avec un sexe ratio de 1.46 en faveur des hommes. La moyenne d’âge était de 33±. La majorité des patients soit 24,42% appartiennent à la tranche d’âge entre 28 et 37 ans. La tuberculose pulmonaire a représenté 71,43% contre 28.57% de tuberculose extrapulmonaire dont la localisation pleurale avait 38,56%. Avec une co-infection au VIH+ de 11,40% et nous pouvons rappeler que cet effectif est celui qui a consulté seulement, que dirons-nous des autres cas qui sont pour l’instant méconnu et dont n’ont pas accès au service de santé ?
Nous estimons que le système pour la prise en charge des patients tuberculeux est encore à améliorer dans la Zone de santé Kenya.
Vous remarquerez que dans nos résultats il n’y a pas des variables comme (profession, niveau d’étude, Etat civil…) c’est tout simplement parce que ces informations ne figurent pas dans le registre des tuberculeux.
SUGGESTIONS
Eu égard aux résultats obtenus dans cette étude, nous suggérons :
Aux autorités sanitaires
- Intensifier les mesures préventives contre la tuberculose tout en travaillant avec toutes les couches de la population car c'est ensemble qu'on peut assister à l'éradication de cette maladie
Au PNLT
- Organiser régulièrement des campagnes d’éducation et de communication pour le changement de comportement des populations qui observent avec négligences les mesures des préventions de la maladie tout en rappelant que la RDC a notifié 202.145 en 2020
- Envisager des formations de renforcement de capacité de personnelles santés prenant en charge les tuberculeux
Aux personnels soignants de la zone de santé Kenya
- Adopter une meilleure méthode de sensibilisation et surtout de l'éducation pour les patients car il ne suffit pas seulement de soigner mais éduquer aussi permettra la réduction des cas dans la zone.
A la population
- Accompagner les patients à suivre le traitement correctement
- Donner aux patients le soutien et toute l’assurance dont ils ont besoin
REFERENCES
Alisjahbana B, Sahiratmadja E, Nelwan EJ et al. (2007), The effect of type 2 diabètes mellitus on the presentation and treat- ment response of pulmonary tuberculosis, Clin. Infect. Dis., 45 (4):428–35
Amarrante, https://www.cairn.info/revue-autrepart-2001-3-page-71.htm
Banyai A.L. (1931), Diabetes and pulmonary tuberculosis, Am. Rev. Tuber., 24:17.
Brändlia, O. et al. Clinique et diagnostic de la tuberculose, dans Forum Med Suisse, 2003.
Beyt E, Ortbalds DW, Santa Cruz DJ. Cutaneous mycobacteriosis: analysis of 34 cases with a new classification of the disease. Medicine. 1980;60:95–109.
Bonnet, M., [New diagnostic tests for tuberculosis in southern countries: from theory to practice in Southern countries]. Revue des maladies respiratoires, 2011.
Catherine W. M. Ong, Paul T. Elkington et Jon S. Friedland, « Tuberculosis, Pulmonary cavitation, and matrix Metalloproteinases », Am J Respir Crit Care Med, American Thoracic Society, vol. 190, no 1, juillet 2014, p. 9–18 (ISSN 1073-449X, DOI 10.1164/rccm.201311-2106pp, lire en ligne).
C Ben Taarit, S Turki et H.Ben Maïz, « La tuberculose ostéoarticulaire en Tunisie : étude rétrospective de 180 cas », Médecine et Maladies Infectieuses, Elsevier BV, vol. 33, no 4, avril 2003, p. 210–214 (ISSN 0399-077X, DOI 10.1016/s0399-077x(03)00009-x, lire en ligne).
C. Marrakchi, I. Maâloul, D. Lahiani, B. Hammami, T. Boudawara, M. Zribi et M. Ben Jemaâ, « Diagnostic de la tuberculose ganglionnaire périphérique en Tunisie », Médecine et Maladies Infectieuses, Elsevier BV, vol. 40, no 2, février 2010, p. 119-122 (ISSN 0399-077X, DOI 10.1016/j.medmal.2009.10.014, lire en ligne).
Christopher Dye, « Global epidemiology of tuberculosis », The Lancet, Elsevier BV, vol. 367, no 9514, mars 2006, p. 938–940 (ISSN 0140-6736, DOI 10.1016/s0140-6736(06)68384-0, lire en ligne).
D. Alland, M. Rowneki, L. Smith, S. Chakravorty, J. Ryan et M. Chancellor (2015) « Xpert MTB/RIF Ultra: a new near-patient TB test with sensitivity equal to culture » dans Conference on Retroviral and Opportunistic Infections, Seattle, WA.
D. Che, « Épidémiologie de la tuberculose », La Revue du Praticien, no 4, avril 2012, p.473–478.
Dr Michel Kaswa Kayomo PNLT https://www.radiokapi.net/2021/03/24/actualite/sante/rdc
Dr Eteni Longondo ministère de la santé RDC https://zoom-eco.net
Dr Jacques Allard, https://www.passeportsante.net/fr/Maux/Problemes/Fiche.aspx?doc=tuber)culose-pm-prevention-de-la-tuberculose
Dr. Robert Koch, « The Aetiology of Tuberculosis » [« L’étiologie de la tuberculose »] [PDF], sur deltaomega.org (consulté le 16 juillet 2010).
Formes cliniques de la tuberculose cutanée. F. Tigoulet, V. Fournier & E. Caume (2001)
Global tuberculosis report », sur World Health Organization (consulté le 9 novembre 2017Guide infection longue durée, tuberculose active, sur Haute Autorité de Santé (consulté le 2 mars 2016) H. Lakhdar, « Tuberculose cutanée », sur Thérapeutique dermatologique, septembre 2005 (consulté le 23 juillet 2012).
J. Andreu, J. Cáceres, E. Pallisa et M. Martinez-Rodriguez, « Manifestations radiologiques de la tuberculose pulmonaire », EMC - Radiologie, Elsevier BV, vol. 2, no 1, février 2005, p. 121–132 (ISSN 1762-4185, DOI 10.1016/j.emcrad.2004.11.005, lire en ligne).
Jad Watfa et Frédéric Michel, « Tuberculose uro-génitale », Progrès en Urologie, vol. 15, no 4, septembre 2005, p. 602–603 (lire en ligne, consulté le 17 mai 2016).
Jeon CY, Murray MB (2008) Diabetes mellitus increases the risk of active tuberculosis: a systematic review of 13 observational studies. PLoS Med 5(7):e152
J Maugein et C Bébéar, « Diagnostic microbiologique de la tuberculose et intérêt de la PCR », Médecine et Maladies Infectieuses, Elsevier BV, vol. 33, mars 2003, p. 153–158 (ISSN 0399-077X, DOI 10.1016/s0399-077x(03)00069-6, lire en ligne)
Kay Codell Carter, « The rise of causal concepts of disease: case histories », sur books.google.fr (consulté le 16 juillet 2010), p. 18
Keertan Dheda, Helen Booth, Jim F. Huggett, Margaret A. Johnson, Alimuddin Zumla et Graham W. Rook, « Lung Remodeling in Pulmonary Tuberculosis », The Journal of Infectious Diseases, Oxford University Press (OUP), vol. 192, no 7, octobre 2005, p. 1201–1209 (ISSN 0022-1899, DOI 10.1086/444545, lire en ligne).
L Boussel, B Marchand, N Blineau, C Pariset, M Hermier, G Picaud, M Emin, A Coulon, P Pagnon, A Rode, J Pin-Leveugle, A Boibieux et Y Berthezène, « Imagerie de la tuberculose ostéo-articulaire », Journal de radiologie, Elsevier Masson, vol. 83, no 9-C1, septembre 2002, p. 1025–1034 (lire en ligne).
L. Jeannin, « Tuberculose pulmonaire et primo-infection tuberculeuse : Épidémiologie, diagnostic, évolution, traitement, prévention », La Revue du praticien, vol. 47, no 1, 1997, p. 97–106.
Li-Jen Wang, Ching-Fang Wu, Yon-Cheong Wong, Cheng Keng Chuang, Sheng-Hsien Chu et Chi-Jen Chen, « Imaging Findings of Urinary Tuberculosis on Excretory Urography and Computerized Tomography », The Journal of Urology, Elsevier BV, vol. 169, no 2, février 2003, p. 524–528 (ISSN 0022-5347, DOI 10.1016/s0022-5347(05)63947-x, lire en ligne)
L. Kivihya-Ndugga et al. « A comprehensive comparison of Ziehl-Neelsen and fluorescence microscopy for the diagnosis of tuberculosis in a resource-poor urban setting », The International Journal of Tuberculosis and Lung Disease, vol. 7, no 12, 2003, p. 1163–1171. Accès direct.
Large outbreak of isoniazid-monoresistant tuberculosis in London, 1995 to 2006: case–control study and recommendations
Matthew Bates et Alimuddin Zumla, « The development, evaluation and performance of molecular diagnostics for detection ofMycobacterium tuberculosis », Expert Review of Molecular Diagnostics, Informa Healthcare, vol. 16, no 3, 17 février 2016, p. 307–322 (ISSN 1473-7159, DOI 10.1586/14737159.2016.1139457, lire en ligne).
Oussama Baker et al ; Tuberculosis ; 25 février 2015
OMS | Co-infection tuberculose/VIH », sur WHO (consulté le 16 juin 2020)
OMS, « Tuberculose : Principaux faits », sur www.who.int (consulté le 1er mars 2021)
Organisation mondiale de la santé, « Global tuberculosis control 2008 », sur who.int, 2008 (consulté le 17 mai 2016).
P Hochedez, V Zeller, C Truffot, S Ansart, É Caumes, R Tubiana, C Katlama, F Bricaire et P Bossi, « Caractéristiques épidémiologiques, cliniques, biologiques et thérapeutiques de la tuberculose ganglionnaire observée chez des patients infectés ou non par le VIH », Pathologie Biologie, Elsevier BV, vol. 51, nos 8–9, octobre 2003, p. 496–502 (ISSN 0369-8114, DOI 10.1016/s0369-8114(03)00145-7, lire en ligne).
Patrick Berche, Une histoire des microbes, Paris, John Libbey Eurotext, 2007 (lire en ligne).
P. Benkimoun, « Tuberculose : malgré les avancées, la maladie tue plus de 4 000 personnes pas jour », sur Le Monde, 28 octobre 2015 (consulté le 17 mai 2016).
Rapport mondial sur la tuberculose, Organisation mondiale de la santé (1993, 2016, 2018, 2019 & 2020)
Rapport sur la tuberculose, Organisation mondiale de la santé Région Africaine (2017, 2018, 2019 & 2020)
Stéphane Henry, Vaincre la tuberculose (1879-1939) : La Normandie en proie à la peste blanche, Publication Universitaire Rouen Havre, 2013, p. 47.
S. Hafaied, B. Hamdi, A. Berraies, H. Cherif, J. Ammar et A. Hamzaoui, « Localisations rares de tuberculose chez l’enfant : à propos de 8 cas », Revue des Maladies Respiratoires, Elsevier BV, vol. 32, janvier 2015, A231–A232 (ISSN 0761-8425, DOI 10.1016/j.rmr.2014.10.377, lire en ligne).
S. Fikal, H. Sajiai, H. Serhane, S. Aitbatahar, H. Rachid, N. Moumen et L. Amro, « Primo-infection tuberculeuse », Revue des Maladies Respiratoires, Elsevier BV, vol. 33, janvier 2016, A158 (ISSN 0761-8425, DOI 10.1016/j.rmr.2015.10.311, lire en ligne).
Sudre, https://www.cairn.info/revue-autrepart-2001-3-page-71.htm
Svetlana Kouznetsova, « Tuberculose : l'épidémie jamais éradiquée », Courrier International, no 1568, 19 novembre 2020, traduction d'un article paru le 19 septembre dans Kommersant.
Thanh, N. P., Khue, P. M., Sy, D. N. et Strobel, M. (2015), Diabète chez les nouveaux cas de tuberculose pulmonaire à Hanoï, Vietnam, Bulletin de la Société de pathologie exotique, 108(5), 337-341, lire en ligne.
Stevenson CR, Critchley JA, Forouhi NG et al. (2007), Diabetes and the risk of tuberculosis: a neglected threat to public health?, Chronic Illn, 3(3):228–45
Sébastien Gobert, « L’Ukraine livrée aux maladies infectieuses », Le Monde diplomatique, vol.
Styblo, https://www.cairn.info/revue-autrepart-2001-3-page-71.htm
Tshamba, July 2014Pan African Medical Journal 17(70):70DOI: 10.11604/pamj.2014.17.70.2445 PubMed Tuberculose », sur who.int (consulté le 16 juin 2020)
Waseem Saeed, « Cavitating pulmonary tuberculosis: a global challenge », Clinical Medicine, Royal College of Physicians, vol. 12, no 1, 1er février 2012, p. 40–41 (ISSN 1470-2118, DOI 10.7861/clinmedicine.12-1-40, lire en ligne).
ANNEXE
FICHE D’EXTRACTION DES DONNEES
« PROFIL EPIDEMIOLOGIQUE DE LA TUBERCULOSE DANS LA ZONE DE SANTE DE LA KENYA »
Sexe :… Age :………
Diagnostic :…………………………………………….
Localisation TEP:……………………………………
![]()
![]() Unité
de traitement :……………………………………
Unité
de traitement :……………………………………
Co-infection TB/VIH : Oui Non
![]()
![]() Date
d’enregistrement :…………………………………
Provenance : dans la Zone Hors zone
Date
d’enregistrement :…………………………………
Provenance : dans la Zone Hors zone
TABLE DES MATIERES
Table des matières
2. PROBLEMATIQUE ET HYPOTHSES DE RECHERCHE
5. DELIMITATION SPACIO-TEMPOREL DU TRAVAIL
PREMIERE PARTIE : CONSIDERATIONS THEORIQUES
I.1 HISTOIRE DE LA TUBERCULOSE
I.2 SYMPTOMES DE LA TUBERCULOSE
I.5 CONTAGION DE LA TUBERCULOSE
I.6 PERSONNES A RISQUE DE LA TUBERCULOSE
I.7 FACTEURS DE RISQUE DE LA TUBERCULOSE
I.8 MESURES PREVENTIVES DE BASE DE LA TUBERCULOSE
I.8 DIAGNOSTIC DE LA TUBERCULOSE
I.9 TRAITEMENT DE LA TUBERCULOSE
I.11 TUBERCULOSE PHARMACORESISTANTE
DEUXIEME PARTIE : CADRE EMPIRIQUE
CHAPITRE II. MATERIELLES ET METHODES
CHAPITRE III. PRESENTATION DES RESULTATS
III.1 Caractéristiques de patients inclus dans cette étude
III.2 Fréquences de la tuberculose chez les patients considérés dans cette étude
CHAPITRE IV. DISCUSSION DES RESULTATS
 Vitrine de la RDC
Vitrine de la RDC