CONTROLE MICROBIOLOGIQUE DES SURFACES INTERNES DES
APPAREILS DE LA CHAINE DE FROID DES BOUCHERIES. (CAS DE LA VILLE DE LUBUMBASHI)
MICROBIOLOGICAL
CONTROL OF INTERNAL SURFACES OF DEVICES IN THE COLD CHAIN OF BUTCHERS. (CASE OF
THE CITY OF LUBUMBASHI)
Kabeya Diyoka
Chadrack 1* | Kasamba Ilunga Eric 2 | Malangu Mposhy
Prosper Emmanuel 2,3 |
1 Nutritionniste| Ecole de Santé Publique | Université de Lubumbashi | R D Congo |
2 Département des Sciences Biomédicales | Faculté de Médecine | Université de Lubumbashi | R D Congo |
3 Faculté de Médecine Vétérinaire | Université de Lubumbashi | R D Congo |
ABSTRACT
The objectives of this work were to identify the
microorganisms forming the resident flora and to determine the level of
microbial contamination of the internal surfaces of the cold chain devices; to
establish the operating temperatures of these devices and to evaluate the
cleaning and disinfection processes of cold chain devices in butcher shops.
This is a cross-sectional descriptive study of a comparative type.
In total, 30 swabs were recovered from the 10 devices
in the cold chain of the butcher shops and showed for Butchery I that: 87% of
the internal surfaces of the devices in the chain were contaminated; The
organisms isolated were S. aureus (54%) and albus (23%), fusarium and A. niger
with 8%, and A. fumagitus (7%); The level of surface contamination for all
isolated organisms was> 1000 CFU / cm2. And for butcher's shop II: 47% of
the internal surfaces of the equipment in the chain were contaminated; The
microorganisms isolated were S. aureus (43%), 29% for K. planticola and 14% for
A. fumagitus and fusarium spp.; The level of surface contamination for all
isolated organisms was> 1000 CFU / cm2. The operating temperature range of
the devices varied between -2 and 6 ° C, with an average of -3.2 ° C in the
first structure against -4.6 and 6 ° C, with an average of -4.7 ° C for the
second structure.
This study has shown that food pathogens and
opportunists can survive on the surfaces of cold chain equipment in butcher
shops and therefore pose a risk of cross-contamination.
Key words: control, microbial contamination, internal surfaces, cold chain devices ABSTRACT
Les objectifs de ce travail étaient d’identifier les microorganismes formant la flore résidente et de déterminer le niveau de contamination microbienne des surfaces internes des appareils de la chaine de froid ; d’établir les températures de fonctionnement de ces appareils et d’évaluer les processus de nettoyage et désinfection des appareils de la chaine de froid des boucheries. Il s’agit d’une étude descriptive transversale de type comparative.
Au total, 30 écouvillons ont été récupérés des 10 appareils de la chaine de froid des boucheries ont montré pour la Boucherie I que : 87% des surfaces internes des appareils de la chaine étaient contaminées ; Les germes isolés étaient le S. aureus (54%) et albus (23%), le fusarium et l’A. niger respectivement avec 8%, et de l’A. fumagitus (7%) ; Le niveau de contamination des surfaces pour tous les germes isolés était > 1000 UFC/cm2. Et pour la boucherie II : 47% des surfaces internes des appareils de la chaine étaient contaminées ; Les microorganismes isolés étaient les S. aureus (43%), 29% pour le K... planticola et 14% pour l’A. fumagitus et le fusarium spp. ; Le niveau de contamination des surfaces pour tous les germes isolés était > 1000 UFC/cm2. La plage des températures de fonctionnement des appareils variait entre -2 et 6 °C, avec une moyenne de -3,2 °C dans la première structure contre -4,6 et 6 °C, avec une moyenne de -4,7 °C pour la deuxième structure.
Cette étude a montré que les agents pathogènes et opportunistes alimentaires peuvent survivre sur les surfaces des appareils de la chaine de froid des boucheries et posent donc un risque de contamination croisée.
Mots clés : contrôle, contamination microbienne, surfaces internes, appareils de la chaine de froid
1. INTRODUCTION
Malgré que la basse température retarde la détérioration des denrées alimentaires, mais même une sous-congélation à une température d'environ 7 ° C n'empêche pas la multiplication de tous les micro-organismes, les aliments réfrigérés sont donc soumis à la détérioration par des moisissures, des levures et des bactéries (Adebayo et al., 2014 ; Bielecki, 2003). La présence des microorganismes au niveau de l’air intérieur et sur les nombreuses surfaces des appareils de la chaine de froid est à l’origine d’effets néfastes à la fois en termes de qualité marchande et de santé publique.
Macias-Rodriguez et al., 2013; Kampmann et al., 2008 ; Otu-Bassey et al., 2017 ont trouvés que 100% des réfrigérateurs inspectés présentent une contamination bactérienne,
32% une contamination fongique et 8% une contamination par les organismes parasites. Les genres de bactéries isolés par ordre décroissant de la fréquence étaient : Staphylococcus aureus 27,3%, Escherichia coli 20,2%, Shigella spp 13,0%, Pseudomonas aeruginosa 11,9%, Aeromonas hydrophilia 8,3%, Salmonella typhi 5,9%, Klebsiella pneumonia 5%, Streptococcus pyogenes 4,7% et Proteus mirabilis 2,3%. Les organismes fongiques isolés étaient candida albicans 54%, penicillium spp 43,2% et aspergilus flavus 2,7% tandis que les parasites détectés étaient Entamoeba histolytica / dispar 50% et Ascaris lumbricoides 50%
La survie et la croissance de micro-organismes dans les appareils de la chaine de froid présente un danger particulier dans les aliments conservés au froid, en particulier dans les produits qui sont consommés sans autre cuisson. Diverses études ont indiqué la possibilité que des produits prêts à consommer subisses une contamination croisée à travers les surfaces du réfrigérateur (Kilonzo-Nthenge et al., 2008). Bien que plusieurs efforts aient été fait pour améliorer la sécurité et la qualité des aliments, les maladies d'origine alimentaire constituent une menace grave pour la santé de millions de personnes (Kilonzo-Nthenge et al., 2008). Environ 76 millions de cas de maladie humaine se produisent aux États-Unis chaque année en raison de maladies d'origine alimentaire (Mead et al., 1999). Beaucoup d'entre eux sont attribuables à une mauvaise alimentation, au stockage, au manque de procédures de manipulation sûres des aliments, à la propreté et la gestion des appareils de la chaine de froid.
(Ryan et al., 1996; Smyth et al., 2006) En RDC, aucune d’étude n’a porté sur l’identification de la flore microbienne des surfaces internes des appareils de la chaine de froid des boucheries. Nous avons donc cherché à identifier les microorganismes formant la flore résidente et déterminer le niveau des contaminations microbienne des surfaces internes des appareils de la chaine de froid des boucheries ; nous avons également étudié les niveaux des températures de fonctionnement des appareils de la chaine de froid des boucheries et l'état d'assainissement et d'hygiène des appareils de la chaine de froid des boucheries de la ville de Lubumbashi.
2. MILIEU, MATERIEL ET METHODES
2.1. Cadre d’étude
Cette étude a été réalisée dans deux boucheries de la ville de Lubumbashi. Lubumbashi est le chef-lieu de la province du Haut-Katanga et la capitale économique de la République Démocratique du Congo (RDC).
2.2. Type d’étude
Il s’agit d’une étude descriptive transversale de type comparative réalisée sur une durée de deux semaines allant du 29 Juin au 11Juillet 2020.
2.3. Collecte d’échantillon
Trente (30) échantillons ont été prélevés sur les surfaces internes 10 appareils de la chaine de froid des boucheries accessibles avec le consentement du promoteur. Le prélèvement se réalisait dans les conditions d’asepsie. Des échantillons ont été prélevés sur le fond et sur deux surfaces à l’aide des écouvillons stériles sec et acheminé vers le laboratoire pour analyse dans l’heure suivant le prélèvement. Nous avons utilisé une fiche de prélèvement des températures pour l’enquête de la chaine de froid et une fiche d’enquête sur le nettoyage et de désinfection des surfaces internes des appareils de la chaine de froid. Un questionnaire a également été administré aux personnels chargés du nettoyage/désinfection pour la récolter des données relatives à notre recherche.
2.4. Milieux de culture
Différents milieux de culture ont été préparés selon spécifications des fabricants. Pour obtenir les bactéries isolées les échantillons ont été inoculés sur CLED Agar, gélose au sel de mannitol et gélose Mac Conkey. Pour obtenir les isolats fongiques, les échantillons ont été inoculés sur Sabouraud Dextrose Agar (SDA).
2.5. Identification des isolats
L'identification initiale des bactéries isolées était basée sur leurs caractéristiques culturelles et morphologiques. Plus loin l'identification était par des caractéristiques biochimiques en utilisant des procédures standard.
a. Coloration GRAM
Un frottis mince d'une culture de 24 heures a été fait sur une glissière sans graisse et fixée thermiquement en passant la glissière rapidement sur une flamme de brûleur Bunsen après séchage à l'air. Le frottis préparé a ensuite été inondé de cristal violet solution pendant environ une minute, rincer à l'eau du robinet ; suivi du mordançage au Lugol (solution d'iode iodoiodurée): étaler le Lugol et laisser agir pendant 1 minute, rincer à l'eau du robinet ; après décoloré à l'alcool (+acétone) : verser goutte à goutte l'alcool ou un mélange alcool-acétone sur la lame inclinée obliquement, et surveiller la décoloration (30 secondes). Rincer à l'eau du robinet ; le frottis a été contre-coloré avec la Safranine pendant 1 minute, lavé à l’eau du robinet ; Sécher la lame à l’air libre ; Observer avec une goutte d'huile à immersion objectif 100 (×1000). Couleur pourpre signifie un organisme Gram positif tout en rose à rouge signifie Gram négatif.
b. Caractéristiques biochimiques des isolats Test de catalase
Déposer sur une lame de verre une ou deux gouttes d'eau oxygénée à 10 volumes.
Prélever à l'aide de l'effilure d'une pipette pasteur un fragment de colonie et dissocier la culture dans l'eau oxygénée. La libération de bulles a immédiatement indiqué un test positif alors qu'il était négatif lorsqu'aucune bulle n'était formée.
2.6. Interprétation
Tableau 1 : Seuils d’acceptabilité des UFC
|
Classe |
|
Satisfaisant |
|
Non satisfaisant |
|
|
Seuils d’acceptabilité UFC |
des |
0-10 U FC/cm2 |
0-1 Log10 UFC/cm2 |
> 10 U FC/cm2 |
> 1 Log10 UFC/cm2 |
Note de service no2007-8275 du 14 novembre 2007 (Bendeddouche and Bensid, 2009)
2.7. Analyse statistique
Les résultats microbiologiques obtenus après incubation ont été saisis à l’aide du logiciel MS Excel 2016 ; traitées et analysées avec des logiciels Excel 2016 et Epi info version 7.2.2.6.
Pour l’analyse et l’interprétation des données, les calculs et les tests statistiques suivants ont été utilisés : la fréquence.
3. RESULTATS 3.1.Niveau de contamination des surfaces et micro-organismes isolés
Tableau I : Répartition de la contamination globale des surfaces par à l’appréciation du nettoyage
![]()
Structure Non Oui Total
|
|
n |
% |
n |
% |
n |
% |
|
Boucherie I |
2 |
20 |
13 |
87 |
15 |
100 |
|
Boucherie II |
8 |
53 |
7 |
47 |
15 |
100 |
|
Total |
10 |
100 |
20 |
100 |
30 |
100 |
Le résultat du tableau n° 1 montre que les points des prélèvements de la structure A sont celles ayant le niveau de contamination le plus élevé avec une fréquence de 87 % et tandis que celles de la structure B présentent une fréquence de 46,67% des zones contaminées.
Dans notre étude, la distribution des bactéries et des moisissures est supérieure à 1000 UFC /cm 2 ou 1 Log10 UFC/cm2 sur toutes les surfaces contaminées. Au niveau de la structure I, 89 % des surfaces internes des frigos sont non acceptables (car > 1 Log10 UFC/cm2) et requièrent un nettoyage/désinfection efficace. Et 83 % des surfaces internes des armoires frigorifiques présentent un niveau d’hygiène non acceptable (> 1 Log10 UFC/cm2) et requièrent un nettoyage/désinfection efficace. staphylococcus (3,47 log10 UFC/cm2), suivie par les aspergillus (0,53 log10 UFC /cm2) et les fusarium (0,27 log10 UFC /cm2 ).
Au niveau de la structure II, 33 % des surfaces internes des chambres froides sont non acceptables (car > 1 Log10 UFC/cm2) et requièrent un nettoyage/désinfection efficace. Et 56 % des surfaces internes des armoires frigorifiques présentent un niveau d’hygiène non acceptables (car > 1 Log10 UFC/cm2) nécessitent un nettoyage/désinfection efficace. Avec une moyenne de 0,80 log10 UFC/cm2 pour le staphylococcus, suivie par les klebsiella planticola (0,51 log10
UFC /cm2), l’Aspergillus fumigatus (0,27 log10 UFC/cm2) et les fusarium (0,26 log10 UFC /cm2).
Tableau II : Répartition des microorganismes isolés des surfaces internes des appareils de la chaine de froid
|
Microorganismes isolés |
Fréquence |
Pourcentage (%) |
|
|
|
Boucherie I Boucherie II |
Boucherie I Boucherie II |
|
|
Bactéries |
10 5 |
77 |
71 |
|
Moisissures |
3 2 |
23 |
29 |
Répartition des microorganismes isolés des surfaces internes des appareils de la chaine de froid, nous avons constaté une prédominance des bactéries (75 %), contre 25 % pour les moisissures. Au niveau de la boucherie I, la contamination bactérienne (77%) et fongique (23%) contre 71% pour la contamination bactérienne et 29% pour la contamination fongique au niveau de la boucherie II.
Tableau III : Répartition globale de souches microbiennes isolées des surfaces internes des appareils de la chaine de froid
|
Microorganismes isolés |
Pourcentage (%) |
|
|
|
Boucherie I |
Boucherie II |
|
Bactéries Staphylococcus aureus |
54 |
43 |
|
Staphylococcus albus |
23 |
0 |
|
Klebsiella planticola |
0 |
29 |
|
Moisissures Aspergillus fumagitus |
7 |
14 |
|
Aspergillus niger |
8 |
0 |
|
Fusarium spp |
8 |
14 |
En termes de pourcentage, les staphylococcus aureus représentent 54 % des germes
dénombrées et contre 7 % d’Aspergillus fumigatus. (Boucherie I) et les staphylococcus aureus représentent 43 % de la flore dénombrée, le Klebsiella planticola (29%) et respectivement 14% pour l’aspergillus fumagitus et le fusarium spp.
3.2.Température des fonctionnements des appareils de la chaine de froid
La température des appareils de la structure I observée variait entre -2 et 6 ° C, avec une température moyenne de -3,2 ° C.

Fig. 1. La répartition des sites de prélèvement selon la température de fonctionnement (Boucherie I)
La plage des températures des appareils de la chaine de froid observée variait entre -4,6 et 6 ° C, avec une température moyenne de -4,7 ° C.
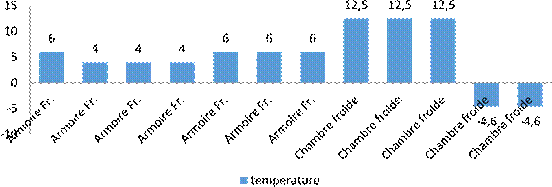
Fig. 2. La répartition des sites de prélèvement selon la température de fonctionnement Distribution des germes selon les points de prélèvement
3.3. Procédure de nettoyage/désinfection
Les réponses des personnes interrogées révèlent que le nettoyage des surfaces internes appareils de la chaine de froid est exécuté chaque matin avant le démarrage des activités et l’ouverture en vue de la vente des denrées alimentaires dans les deux boucheries, et à la fin de chaque journée pour remettre les surfaces à l’état propre dans la boucherie I ; L'éponge (lavettes), la raclette et les sceaux sont les instruments de nettoyage le plus souvent utilisés dans les deux structures. Les produits de nettoyage/désinfection utilisées contenaient comme principes actifs, l’acide acétique et l’eau de Javel.
4. DISCUSSION 4.1.Niveau de contamination des surfaces
Les points des prélèvements de la structure A sont celles ayant le niveau des contaminations les plus élevés avec une fréquence de 87 % et tandis que celles de la structure B présentent une fréquence de 46,67% des zones contaminées. Macias-Rodriguez et al., 2013; Kampmann et al., 2008 ; Otu-Bassey et al., 2017 ont trouvés que 100% des réfrigérateurs inspectés présentent une contamination bactérienne, 32% une contamination fongique et 8% une contamination par les organismes parasites.
Au niveau de la structure I, 89 % des surfaces internes des frigos sont non acceptables (car > 1 Log10 UFC/cm2) et requièrent un nettoyage/désinfection efficace. Et 83 % des surfaces internes des armoires frigorifiques présentent un niveau d’hygiène non acceptable (> 1 Log10 UFC/cm2) et requièrent un nettoyage/désinfection efficace. Au niveau de la structure II, 33 % des surfaces internes des chambres froides sont non acceptables (car > 1 Log10 UFC/cm2) et requièrent un nettoyage/désinfection efficace. Et 56 % des surfaces internes des armoires frigorifiques présentent un niveau d’hygiène non acceptables (car > 1 Log10 UFC/cm2) nécessitent un nettoyage/désinfection efficace.
Ce résultat est similaire avec celle ZICKRICK et al., 1995, qui ont constaté que 17,2% des réfrigérateurs domestiques en Allemagne contenaient > 1000 UFC / m 3. Et ne sont pas cohérents avec ceux trouvés par Altunatmaz et al. qui ont trouvés que des bactéries psychrotrophes dans tout l'air échantillonné étaient <200 UFC / m 3 (Altunatmaz et al., 2012).
Au niveau de la Boucherie I, les S. aureus représentent 54 % des germes dénombrées, suivi des S. albus (23%), de l’A. niger et du fusarium spp (8%), A. Fumagitus (7 %) ; par contre au niveau de la boucherie II, les S. aureus représentent 43 % de la flore dénombrée, le K.planticola (29%) et respectivement 14% pour l’aspergillus fumagitus et le fusarium spp.
Macias-Rodriguez et al., 2013; Kampmann et al., 2008 ; Otu-Bassey et al., 2017 ont rapportés que les genres bactériens isolés par ordre décroissant de la fréquence étaient : Staphylococcus aureus 27,3%, Escherichia coli 20,2%, Shigella spp 13,0%, Pseudomonas aeruginosa 11,9%, Aeromonas hydrophilia 8,3%, Salmonella typhi 5,9%, Klebsiella pneumonia 5%, Streptococcus pyogenes 4,7% et Proteus mirabilis 2,3%. Les organismes fongiques isolés étaient candida albicans 54%, penicillium spp 43,2% et aspergilus flavus 2,7% tandis que les parasites détectés étaient Entamoeba histolytica / dispar 50% et Ascaris lumbricoides 50%.
Otu-Bassey et al., 2017 ; Oluwafemi et al., 2015. ont isolé d’autres espèces des bactéries et les champignons dans les réfrigérateurs domiciles, Staphylococcus aureus, Escherichia coli, Bacillus subtilis, Enterobacter spp., Klebsiella spp. et Shigella spp., Aspergillus flavus, A. niger, A. fumigatus, Saccharomyces cerevisae et Rhizopus spp. Ces organismes indésirables peuvent avoir pénétrés dans les appareils de la chaine de froid à partir d'aliments crus non lavés, aliments mal emballés (viandes, œufs et lait), mains sales, à travers une porte de réfrigérateur ouverte, fluctuation des températures, et les surfaces des conteneurs impropres introduites dans le réfrigérateur.
4.2. La température de fonctionnement des appareils de la chaine de froid
La température est l'un des principaux facteurs de contrôle de la qualité et de la sécurité sanitaire des aliments en raison de son influence sur les taux de croissance microbienne. Malgré le fait que la basse température peut réduire le taux de croissance de nombreuses espèces de micro-organismes, il a été signalé que les micro-organismes psychrotrophes peuvent se développer à des températures de réfrigération normales (Marklinder et al., 2004). Pour la boucherie I, La plage des températures variait entre -2 et 6 ° C, avec une température moyenne de -3,2 ° C. Pour la boucherie II, La plage des températures variait entre -4,6 et 6 ° C, avec un température moyenne de -4,7 ° C.
L'OMS recommande, la température de conservation des aliments à un maximum de 5 ° C au réfrigérateur (OMS, 2007). Garrido et al., 2010, a signalé qu'une baisse de température est importante pour retarder la croissance des agents pathogènes et autres microorganismes pendant la durée de conservation du produit, en particulier une fois le produit acheté et sous la responsabilité des producteurs ou des consommateurs de denrées alimentaires.
4.3.Processus de nettoyage/désinfection
Pour éliminer un maximum de micro-organismes, il convient de réaliser un nettoyage
avec un détergent, afin d’éliminer la majeure partie des souillures présentes sur les surfaces, puis de désinfecter.
Les propriétés antimicrobiennes de l’acide acétique sont attribuées respectivement à leur teneur en acide acétique et en acide citrique (Yang et al., 2009). On suppose que ces acides organiques traversent la membrane cellulaire des bactéries et que la libération de protons (H+) dans les cellules entraîne leur mort (Bjornsdottir et al., 2006). L’eau de Javel, un bactéricide, un fongicide testé en laboratoire d’après la norme EN 13697 après un temps de contact de 15 munîtes. Utilisée à une concentrée élevée, l’eau de javel risque d’agresser la surface sur laquelle elle a été appliquée et ainsi provoquer des crevasses favorables à l’implantation des microorganismes.
Les réponses sur la fréquence du nettoyage/désinfection obtenues dans notre enquête se rapprochent de celles obtenues dans l’enquête INCA réalisée par (Volatier, 2000) et (Lagendijk et al., 2010) dans l’enquête sur les pratiques des consommateurs et recommandations en matière d’hygiène. En effet, 56% et 64 % des répondants déclaraient nettoyer leur réfrigérateur au moins une fois par trimestre.
L'éponge (lavettes), la raclette et les sceaux sont les instruments de nettoyage le plus souvent utilisés dans les deux structures. Utiliser une même éponge pour nettoyer à la fois les appareils de la chaine de froid, et d’autres surfaces, favorise la circulation des micro-organismes dans la structure. De plus, une éponge fréquemment utilisée et ainsi presque toujours humide est de ce fait très chargée en micro-organismes (Josephson et al., 1997). Le lavage à l’éponge peut donc constituer un mode de contamination des appareils de la chaine de froid (Mattick et al., 2003). L’utilisation des raclettes et de la brosse à main, agressif pour les surfaces, est à proscrire car susceptible de provoquer des rayures et ainsi de favoriser la rétention des souillures et des micro-organismes.
CONCLUSION
Cette étude a montré que les agents pathogènes et opportunistes alimentaires peuvent survivre sur les surfaces des appareils de la chaine de froid des boucheries et posent donc un risque de contamination croisée. Au travers nos résultats, nous avons établi que les appareils de la chaine de froid des boucheries pour le stockage des aliments ne sont pas aussi stériles. Les entérobactéries ainsi que les moisissures constituent la flore résidente des surfaces internes des appareils de la chaine de froid dans notre milieu, d’où l'importance du contrôle de la température de fonctionnement, des régimes de nettoyage/désinfection efficaces réguliers qui doivent être communiquée aux boucheries afin d'assurer la qualité, et la sécurité des surfaces mises à la disposition de la fonction production et la vente des denrées alimentaires.
REFERENCE
Adebayo, C.O., Aderiye, B.I., Akpor, O.B., 2014. Assessment of bacterial and fungal spoilage of some Nigerian fermented and unfermented foods. Afr. J. Food Sci. 8, 140–147.
Altunatmaz, S.S., Issa, G., Aydin, A., 2012. Detection of airborne psychrotrophic bacteria and fungi in food storage refrigerators. Braz. J. Microbiol. 43, 1436–1443.
Bendeddouche, B., Bensid, A., 2009. Contrôle de L’efficacité des Opérations de Nettoyage et de La Désinfection des Équipements dans un Abattoir de Volailles en Algérie. Eur. J. Sci. Res. 27, 181–187.
Bielecki, J., 2003. Emerging food pathogens and bacterial toxins. Acta Microbiol. Pol. 52, 17– 22.
Bjornsdottir, Kj., Breidt, F., McFeeters, R.F., 2006. Protective effects of organic acids on survival of Escherichia coli O157: H7 in acidic environments. Appl. Environ. Microbiol. 72, 660–664.
Garrido, V., García-Jalón, I., Vitas, A.I., 2010. Temperature distribution in Spanish domestic refrigerators and its effect on Listeria monocytogenes growth in sliced ready-to-eat ham. Food Control 21, 896–901.
Josephson, K.L., Rubino, J.R., Pepper, I.L., 1997. Characterization and quantification of bacterial pathogens and indicator organisms inhousehold kitchens with and without the use of a disinfectant cleaner. J. Appl. Microbiol. 83, 737–750.
Kampmann, Y., De Clerck, E., Kohn, S., Patchala, D.K., Langerock, R., Kreyenschmidt, J., 2008. Study on the antimicrobial effect of silver-containing inner liners in refrigerators. J. Appl. Microbiol. 104, 1808–1814.
Kilonzo-Nthenge, A., Chen, F.-C., Godwin, S.L., 2008. Occurrence of Listeria and Enterobacteriaceae in domestic refrigerators. J. Food Prot. 71, 608–612.
Lagendijk, E., Asséré, A., Derens, E., Carpentier, B., 2010. Réfrigération domestique: enquête sur les pratiques des consommateurs et recommandations en matière d’hygiène.
Macias-Rodriguez, M.E., Navarro-Hidalgo, V., Linares-Morales, J.R., Olea-Rodriguez, M.A., Villarruel-López, A., Castro-Rosas, J., Gomez-Aldapa, C.A., Torres-Vitela, M.R., 2013. Microbiological safety of domestic refrigerators and the dishcloths used to clean them in Guadalajara, Jalisco, Mexico. J. Food Prot. 76, 984–990.
Marklinder, I.M., Lindblad, M., Eriksson, L.M., Finnson, A.M., Lindqvist, R., 2004. Home storage temperatures and consumer handling of refrigerated foods in Sweden. J. Food Prot. 67, 2570–2577.
Mattick, K., Durham, K., Domingue, G., Jørgensen, F., Sen, M., Schaffner, D.W., Humphrey, T., 2003. The survival of foodborne pathogens during domestic washing-up and subsequent transfer onto washing-up sponges, kitchen surfaces and food. Int. J. Food Microbiol. 85, 213–226.
Mead, P.S., Slutsker, L., Dietz, V., McCaig, L.F., Bresee, J.S., Shapiro, C., Griffin, P.M., Tauxe, R.V., 1999. Food-related illness and death in the United States. Emerg. Infect. Dis. 5, 607.
Oluwafemi, F., Akpoguma, S., Oladiran, T., Kolapo, A.L., 2015. Microbiological Quality of Household Refrigerators in Three Cities South-West of Nigeria [WWW Document]. URL https://www.semanticscholar.org/paper/Microbiological-Quality-of-HouseholdRefrigerators-Oluwafemi-Akpoguma/deb64f5b471e9053a4b4acec6783823b2849326e (accessed 3.30.20).
Organization, W.H., 2007. Directives relatives à la préparation, à la conservation et la manipulation dans de bonnes conditions des préparations en poudre pour nourrissons.
Otu-Bassey, I.B., Ewaoche, I.S., Okon, F.B., Ibor, U.A., 2017. Microbial contamination of house hold refrigerators in Calabar Metropolis-Nigeria. Am J Epidem Infect Dis 51, 1– 7.
Ryan, M.J., Wall, P.G., Gilbert, R.J., Griffin, M., Rowe, B., 1996. Risk factors for outbreaks of infectious intestinal disease linked to domestic catering. Commun. Dis. Rep. CDR Rev. 6, R179-83. Smyth, D.S., Kennedy, J., Twohig, J., MIAJLOVIĆ, H., Bolton, D., Smyth, C.J., 2006. Staphylococcus aureus isolates from Irish domestic refrigerators possess novel enterotoxin and enterotoxin-like genes and are clonal in nature. J. Food Prot. 69, 508– 515.
Volatier, J.-L., 2000. Enquête INCA individuelle et nationale sur les consommations alimentaires. Tec Doc Ed. Paris Ed.
Yang, H., Kendall, P.A., Medeiros, L., Sofos, J.N., 2009. Inactivation of Listeria monocytogenes, Escherichia coli O157: H7, and Salmonella typhimurium with compounds available in households. J. Food Prot. 72, 1201–1208.
ZICKRICK, K., Wittenberg, U., Kiewel, S., 1995. Beitrag zum mikrobiellen Status der inneren Oberflächen und der Luft von Haushaltskühlschränken. Arch. Für Leb. 46, 91–94.
Appendices
UFC : Unités Formant Colonies cm : centimètre
S. : Staphylocoques
A. : Aspergillus
K. : Klebsiella
Spp : species plurimae
CLED : Cystine Lactose Electrolyte Deficient
SDA : Sabouraud Dextrose Agar
RDC : République Démocratique du Congo
OMS : Organisation Mondiale de la Santé



