IN MEMORIAM
A notre défunt père GUIMARANZI Emmanuel KANZA. Que ce travail pour lequel tu as investi honore ton âme.
DEDICACE
A notre mère AMBA LOBALO Georgine, pour non seulement nous avoir donné la vie, mais aussi pour tant d’affection et d’amour, ainsi que des sacrifices consentis pour nous assurer une bonne éducation.
A nos frères et sœurs : Zecka, Pamela, Bénédicte, Joël, Emmanuel, Sophonie, Papa, Hénock, David, Omega, Methe, Judith, Henriico, Auguste, Oberoon ;
A mes enfants ; Coeurtus CELIA, Cyntiche, Précieux ;
A notre fiancé Paulin KILABI pour tant d’amour et de soutien.
Choubine GUIMARAES
REMERCIEMENTS
A notre Seigneur et Sauveur Jésus-Christ, dont l’implication a été manifeste tout au long de notre vie parsemée de tant d’embuches et, plus encore durant nos études universitaires.
Au terme de notre formation à l’Université Technologique Bel Campus, Faculté de Médecine, nous rendons grâce à l’Eternel, notre Dieu, maître de temps et de circonstance, pour son assistance sans laquelle ce jour ne serait pas arrivé.
Qu’il nous soit permis de remercier les personnes dont l’assistance de loin ou de près nous a été d’un grand bénéfice.
Nous exprimons toute notre gratitude à toutes nos autorités académiques de l’Université Technologique Bel Campus, pour la construction de cet édifice que nous sommes. Votre contribution à notre formation nous sera inoubliable.
Nous sommes particulièrement redevable au Professeur Docteur BOBANGA LENGU Thierry, malgré ses multiples occupations, était toujours là pour nous guider.
A nos tantes Jacquie, Joséphine, Marie Thérèse, Emiliame, Janette.
A nos tantes paternelles Josée, Bibi, Emiliane, Charlotte, Jide, pour tous les bienfaits.
A nos oncles Professeur Jeannot WINGENGA-w- EPENDO, Guymo, Eva, Jean-Pierre, Jeudi, Patrick.
Aux collègues de promotion, pour leur soutien moral, physique et intellectuel durant tout le temps de nos études, spécialement à Ange, Théo, Elvier, Patrick.
Choubine GUIMARAES
LISTE DES ABREVIATIONS
% : Pourcentage
A Duodenale : Ankylostome Duodenale
E- Coli : Entamoeba coli
L1 : Larve rhabditoïde au stade 1
L2 : Larve rhacuglyloïde au stade 2
L3 : Larve stacuglyloïde en filariforme
A Lumbricoïde : Ascaris Lumbiicoïdes
n : Nombre
N : Americanus : Necator Americanus
OMS : Organisation Mondiale de la Santé
RDC : République Démocratique du Congo
S. Stercoralis : Strongyloïdes stercoralis
T. Trichiura : Trichuris trichiura
T° : Température
VIH : Virus Immuno Humain
LISTE DES TABLEAUX
|
|
Pages |
|
Tableau 1 : Répartition de cas selon les tranches d’âge……… Tableau 2 : Répartition selon la profession……………………….. Tableau 3 : Répartition selon le lieu d’habitation………………. Tableau 4 : Prévalence des parasites selon les résultats……… Tableau 5 : Prévalence des géohelminthes selon les espèces. Tableau 6 : Répartition des autres parasites du tube digestif… Tableau 7 : Prévalence suivant le parasitisme…………………...
|
…….28 …….29 …….30 …….31 …….31 …….31 ……32 |
LISTE DES FIGURES
|
|
Pages |
|
Figure 1. Œuf de Trichuristrichiura(http : //www.dpd.cdc.gov/dpdx) Figure 2. Cycle évolutif de Trichuristrichiura (http : //www.dpd.cdc.gov/dpdx) Figure 3. Œufs fécondé et non fécondé d’A. lombricoïdes(http : //www.dpd.cdc.gov/dpdx) Figure 4. Cycle d’Ascaris lombricoïdes (http : //www.dpd.cdc.gov/dpdx) Figure 5.Œufd’Ankylostome (http: //www.dpd.cdc.gov/dpdx) Figure 6. Cycle d’Ankylostome(http: //www.dpd.cdc.gov/dpdx) Figure 7. Cycle de S. stercoralis(http : //www.dpd.cdc.gov/dpdx) Figure 8 : Répartition selon le sexe.
|
………..6 ………..7
……..…9
……...11 ……...15 ….…..16 ….…..20
……...29 |
TABLE DES MATIERES
0.3. JUSTIFICATION DE L’ETUDE :
I.2. CARACTERES GENERAUX DES NEMATODES
I.4. LOCALISATION CHEZ L’HOMME
I.5.1. Trichuristrichiura ou Trichocéphale
I.5.2. Ascarislumbricoides ou Ascaris
I.5.3. Ankylostoma sp ou ankylostomes
I.5.4. Strongyloides stercoralis ou anguillule
Chapitre II : MATERIELS ET METHODES
II.1. NATURE ET PERIODE DE L’ETUDE
II.3.1. Critères d’inclusion :
II.5.1. Examen des selles aprèsconcentration (Ritchie modifié)
III.1. Paramètres socio-démographiques :
III.2. Prévalence des géohelminthes
RESUME
Problématique : Les géohelmintes sont des parasites cosmopolites, prédominant dans les pays en voie de développement où différents facteurs concourent à leurs transmissions et menacent 10 à 90% de la population. La charge globale de morbidité est estimée pour A. Lumbricoïdes. T. Trichiura et Aduodénal à 44,7 millions.
Objectif : Détermination de la prévalence des géohelmites.
Méthodologie : Une étude transversale analytique a été menée auprès de 80 personnes de juillet au décembre 2017.
Résultats : 80 échantillons de selles ont été récoltés et examinés. La prévalence des géohelmintus était de 62,7%. Les espèces suivantes ont été trouvées :
A. Lumbicoïde (50%) T. Trichiura (25%)
A. Duodénal (6,25%)
Conclusion : Les géohelminthes constituent un problème non seulement pour les enfants, mais aussi pour les adultes, vue la prévalence de notre étude.
0. INTRODUCTION
0.1. PROBLE MATIQUE
Les parasitoses intestinales semblent de nos jours susciter de moins en moins d’intérêt à cause du détournement justifie des ressources disponibles vers de priorités plus récentes telles que le sida(1).
Les géo helminthes sont des nématodes (vers ronds) dont les œufs passent obligatoirement par le sol pour leur maturation(2). Les principales espèces de géo helminthes qui infestent l’homme appartiennent à l’embranchement des nématodes, les espèces les plus courantes sont les suivantes : Ascaris Lumbricoïdes ; Trichuristrichura, Necator Americanus et Ancylostoma Duodénale(2).
Plus de deux milliards de personnes sont menacées de part le monde et un milliard sont infectées dont 447 millions pour les trois principaux géohelminthes (ascaridiose, trichiurose, ankylostomiase) avec 647 années perdues. (3) Elles sont responsables de 135000décés par année (3).
Ces affections ne doivent pas être négligées, compte tenu des problèmes de santé publique qu’elles posent à nos pays en développement (1). Ils affectent surtout les enfants en âge préscolaire et scolaire.Ils sont responsables des problèmes sanitaires graves comprenant entre autres l’occlusion intestinale, les troubles nutritionnels, la détérioration de l’état de croissance, déficit en vitamine A et de capacités intellectuelles, troubles de mémoires, etc. (4).
Selon l’OMS, les géohelminthiases constituant un problème majeur de santé publique. La majorité des sujets atteints proviennent des pays en développement. (5) L’importance des géohelminthiases est sous-estimée dans le monde alors que cette maladie, d’après les experts est en pleine expansion(6).
Les géohelminthiases sont endémiques dans les régions tropicales et subtropicales humides. Selon l’OMS, 266,4millions d’enfants d’âge préscolaire et 609millions d’enfants d’âgescolaire dans 112pays avaient besoin d’une chimio prévention des géohelminthiases(5).
En RDC, en titre d’exemple, les dernières publications originales sur la prévalence datent des années1969et1972en dehors d’uneméta analyse publiée par le professeur MULUMBA en 2009(3) le mémoire de fin de spécialisation de Dr NUNDUla même année(7) d’où l’importance d’actualiser les données pour un meilleur contrôle et prise en charge du problème des géohelminthes.
Quand on évalue l’importance des géohelminthes et des programmes antihelminthiques, les facteurs à prendre en considération sont ceux qui interviennent dans la transmission de la maladie. Entre autre : le niveau socio-économique bas, les conditions d’hygiène alimentaire et sanitaire précaires, l’inaccessibilité en eau potable, le niveau bas des scolarisations des parents, la profession des agriculteurs et des fermiers(4).
Etant donné que les données sur les facteurs favorisants sont fragmentaires en RDC, cette étude s’est proposé de les analyser en vue de formuler une meilleure politique de lutte contre ces affections.
Le but principal de cette étude est de déterminer l’ampleur des géohelminthes le long de la rivière Kalamu.
0.2. OBJECTIF
· Général : contribuer à l’amélioration de la prise en charge des géohelminthes.
· Spécifique :
ü déterminer la prévalence des géohelminthes chez les individus vivant le long de la rivière Kalamu ;
ü déterminer le type et la fréquence des géohelminthes ;
ü déterminer les facteurs sociodémographiques liés à la transmission des géohelminthes dans cette tranche de la population ;
ü formuler les recommandationsaux autorités sanitaires.
0.3. JUSTIFICATION DE L’ETUDE :
La localisation et la précarité de cette population habitant le long de la rivière Kalamu, il serait donc important d’évaluer la prévalence des géohelminthes.
I.1. DEFINITION
Les géohelminthes sont des nématodes (vers ronds) dont les œufs passent obligatoirement par le sol pour leur maturation. Il s’agit de Trichuristrichiura, Ascaris lumbricoides, Ankylostomasp (Ankylostoma duodenale, Necator americanus) et Strongyloides stercoralis.
Les helminthes sont des parasites appartenant à plusieurs embranchements du règne animal regroupant tous les vers, c'est-à-dire les animaux à symétrie bilatérale, dépourvus d’appendices articulés et au corps mou, plus ou moins allongé. En réalité, il y a une difficulté de trouver une définition globale. C’est pourquoi ils sont définis par des caractères négatifs suivants : l’absence de segmentation, de cavité générale vraie, d’organes respiratoires, de vaisseaux sanguins et de pattes.
Le terme helminthe recouvre à l’heure actuelle huit embranchements : Plathelminthes, Acanthocéphales, Némertiens, Némathelminthes, Annélides, Préapuliens, Sipunculiens et Echiuriens.
I.2. CARACTERES GENERAUX DES NEMATODES
Ce sont des vers de forme cylindrique, allongés, fusiformes dépourvus de segmentation. Ils ont des sexes séparés, le mâle étant plus petit que la femelle avec une curvature ventrale de son extrémité caudale.
En outre, on leur trouve : un Tégument, un Système digestif, un Système reproducteur, un Système nerveux, un Système excréteur.
I.3. CYCLE EVOLUTIF
Il est relativement simple en général. A l’intérieur de l’œuf, l’embryon se transforme en larve et sort de l’œuf. Le passage du stade embryonnaire au stade larvaire est défini par l’apparition d’organes internes. La larve ressemble à l’adulte et subit 4 mues avant de devenir adulte. Les premières mues se font à l’intérieur de l’œuf et, en général, la larve L3 est infectante.
La plupart des nématodes sont ovipares, mais quelques-uns sont vivipares tels que le Trichinellaspiralis et les filaires.
I.4. LOCALISATION CHEZ L’HOMME
Trois localisations principales sont connues chez l’homme. Il s’agit de :
ü Nématodes du tube digestif : Enterobius vermicularis, Trichuristrichiura, Ascaris lumbricoides, Ancylostoma duodenale/Necator americanus, Strongyloides stercoralis, Physaloptera caucasica ;
ü Nématodes du tube digestif et des tissus : Trichinellaspiralis ;
ü Nématodes des tissus : Filaires.
I.5. SYSTEMATIQUE
I.5.1. Trichuristrichiura ou Trichocéphale
I.5.1.1. Epidémiologie
C’est un parasite cosmopolite qui est plus fréquent dans les pays chaudset humides. Il parasite surtout les enfants et est la troisième verminose après les ankylostomes. Il y a environ 800millions de personnes qui sont infectées (Vandepitte 1998).
L’embryonnement des œufs se fait obligatoirement sur le sol et sa survie est prolongée. Son réservoir est donc tellurique et les œufs sont éliminés avec les déjections humaines. C’est une affection liée au péril fécal humain.
La contamination se fait par l’eau de boisson, les mains et les crudités souillées par des œufs embryonnés (maladie des mains sales). Ceux-ci sont tués par la chaleur, l'ensoleillement direct et la dessiccation.
I.5.1.2. Morphologie
· Adulte
C’est un ver blanc rosé à rougeâtre, les 2/3 antérieures fins (1 mm de diamètre) et le 1/3 postérieur épais contenant les organes génitaux (3 mm de diamètre).
Le mâle mesure 3 à 4 mm avec une extrémité postérieure en crosse.
La femelle mesure 4 à 5 mm avec une extrémité postérieure obtuse.
· Œuf
Il est en forme de citron, avec un bouchon muqueux proéminent à chaque pôle, et une coque double dont l’externe est lisse et brune ; l’interne est jaune. Il mesure 50-60 µm x 25-30 µm.
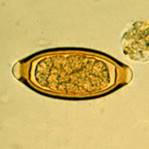
Figure 1. Œuf de Trichuristrichiura(http : //www.dpd.cdc.gov/dpdx)
I.5.1.3. Habitat
La lumière du caecum constitue la niche écologique du trichocéphale, dans les parties adjacentes de l’intestin. La partie filiforme qui est antérieure est enfoncée dans la muqueuse et la sous muqueuse de l’intestin.
L’infection massive se fait au niveau du rectum.
I.5.1.4. Cycle
Les œufs non embryonnés sont éliminés dans les selles. Dans le sol, ils deviennent embryonnés (L1: infectants) après 2 à 4 semaines. Après ingestion des œufs par les aliments (eau, crudités) ou les mains souillées, ils éclosent dans la muqueuse de l’intestin grêle et libèrent une larve. L’évolution larvaire et les mues se font au niveau de l'intestin grêle en 2 à 3 semaines (stades L2, L3, L4), puis les adultes descendent et s’installent dans le côlon.
Les œufs apparaissent dans les selles 60 à 70 jours après l’infection. Le ver pond 3.000 à 30.000 œufs par jour et peut vivre 5 à 10 ans
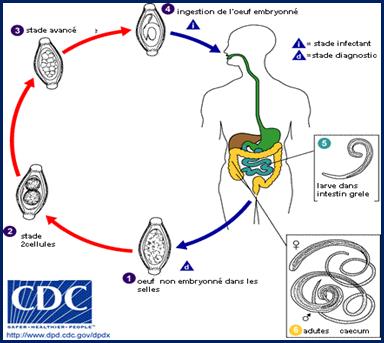
Figure 2. Cycle évolutif de Trichuristrichiura (http : //www.dpd.cdc.gov/dpdx)
I.5.1.5. Pathogénie
La pathogénie est celle de l’effet de masse. On estime qu’en dessous de 400 vers, généralement le sujet est asymptomatique.
I.5.1.6. Symptômes
L’infection est souvent asymptomatique. L’infection massive, spécialement chez les jeunes enfants peut occasionner des troubles digestifs (douleur abdominale, diarrhée muqueuse, prolapsus rectal et anémie) et un possible retard de croissance.
Les complications les plus courantes sont l’appendicite et l’anémie hypochrome.
I.5.1.7. Stade diagnostic
C’est l’œuf ovoïde en forme de tonneau ou de citron, mesurant 50 µm sur 20 µm, de couleur jaune-brun. Sa coque très épaisse est interrompue aux 2 extrémités par un bouchon muqueux.
I.5.1.8. Diagnostic
Le diagnostic est microscopique par l’examen à frais de selles. Il doit être quantitatif : 1 œuf dans une préparation standard (2 mg) représente 10 vers adultes.
En cas de prolapsus, les vers adultes sont observés au niveau de la muqueuse rectale.
I.5.1.9. Traitement
· mébendazole (vermox®) cure de 600mg en 2 prises de 100mg pendant 3jours ;
· albendazole (zentel®) cure de 400mg en une prise ;
· ivermectine (Mectizan®) en dose unique ; 150 μg par kg.
I.5.1.10. Prévention
Elle est basée sur la propreté des mains et des aliments, la lutte contre le péril fécal et le traitement annuel par l'ivermectine ou semestriel par l'albendazole. L’utilisation des latrines est à promouvoir.
I.5.2. Ascarislumbricoides ou Ascaris
I.5.2.1. Epidémiologie
L’ascaris est un parasite cosmopolite. C’est l’helminthiase la plus commune avec une prévalence élevée dans les régions tropicales, subtropicales et les endroits où l’hygiène fécale et alimentaire est défectueuse. Environ 1/3 de la population mondiale s’infecte. Sa prévalence peut atteindre 70% des enfants (Vandepitte 1998).
I.5.2.2. Morphologie
· Adulte
C’est un Ver blanc rosé, élastique. Il possède une bouche pourvue de 3 lèvres coupantes.
Son organisation interne est du type polymaire à grandes cellules musculaires.
Le mâle mesure 15 à 20 cm de long et 0.3 cm de diamètre, avec une extrémité postérieure en crosse, 2 spicules brunâtres. La femelle mesure 20-45 cm, a un diamètre de 0.5 cm, une extrémité postérieure rectiligne et une vulve ventrale au 1/3 antérieur
· Œuf
Il est ovoïde et possède une double coque ; l'externe est brune et mamelonnée, l'interne lisse et jaunâtre. Il mesure 50-70 µm x 45-50 µm. Il est non embryonné à la ponte.
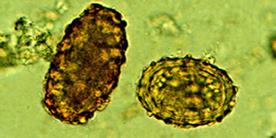
Figure 3. Œufs fécondé et non fécondé d’A. lombricoïdes(http : //www.dpd.cdc.gov/dpdx)
I.5.2.3. Habitat
La lumière de l’intestin grêle est l’environnement spécifique de l’Ascaris. Il a une grande tendance à la migration vers l’appendice, les canaux biliaires ou le canal de Wirsung, le tube d’Eustache, la paroi intestinale et le foie.
I.5.2.4. Cycle
Les œufs non embryonnés sont éliminés dans les selles. Dans le sol, ils deviennent infectants après 2 à 4 semaines.
Les œufs non fécondés peuvent être ingérés mais ne sont pas infectants. Ceux qui sont fécondés subissent une maturation (larves L1 puis L2 qui reste dans l'œuf) et deviennent infectants après 18 jours à plusieurs semaines, selon les conditions de l’environnement (humidité, chaleur, sol ombragé).
Les œufs infectants sont ingérés, la larve éclot dans le duodénum, pénètre dans la muqueuse ; et par la voie portale, atteint le foie, le système cave, le cœur droit et le poumon. La larve poursuit sa maturation dans les poumons (10 à14 jours), perce la paroi de l’alvéole, remonte les bronches et la trachée, arrive à la glotte où elle est déglutie et se retrouve dans l’intestin.
Après une 4è mue elle devient adulte et les œufs apparaissent dans les selles 2 à 3 mois après l’infection.
Une femelle peut libérer jusqu’à 200.000 œufs par jour qui sont éliminés avec les selles.
Le ver adulte ne vit pas plus de 2 ans.
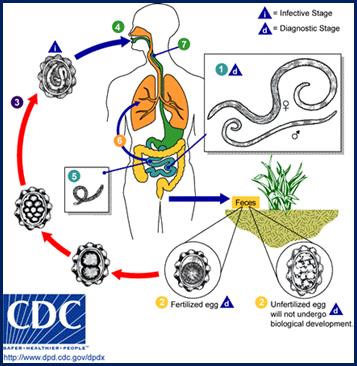
Figure 4. Cycle d’Ascaris lombricoïdes (http : //www.dpd.cdc.gov/dpdx)
I.5.2.5. Pathogénie
La pathologie est causée par la toxine secrétée par le parasite (effet de masse).
L’Ascaris provoque la spoliation protéique (effet de masse).
L’action mécanique due à la migration des vers est exacerbée par le déséquilibre du rapport entre le mâle et la femelle.
Il entraîne également une allergie (syndrome de Loeffler).
I.5.2.6. Symptômes
La maladie n’a souvent pas de symptômes aigus. Elle comprend 2 phases :
· Phase d'invasion :
Elle correspond au passage pulmonaire à la première semaine de la maladie.
La pathogénie se fait par action toxique, allergique, mécanique, traumatique et bactériologique.
Elle est caractérisée par le syndrome de Loeffler: fièvre, toux sèche, dyspnée, crachats, manifestations allergiques, opacité radiologique transitoire.
· Phase d'état :
Elle se caractérise par la présence des adultes dans le tube digestif. Les signes cliniques dépendent du nombre de vers et des traumatismes causés. Les troubles gastro-intestinaux suivants peuvent être observés: douleur abdominale, transit accéléré, vomissements.
On peut observer également des troubles nerveux : irritabilité, insomnie, sialorrhée nocturne.
I.5.2.7. Diagnostic
En phase d'invasion
· diagnostic d'orientation : opacité radiologique, hyperéosinophilie, hyperleucocytose ;
· diagnostic direct : impossible ;
· diagnostic indirect : possibilité de recherche des anticorps sériques.
En phase d'état
· diagnostic direct : Il se fait par grâce à une coprologie par un examen à frais ou après concentration. Au microscope, on observe un œuf de 60 x45 µm, non embryonné à l'émission.
Un œuf dans une préparation standard (2 mg) = 0,5 adulte.
Il y a possibilité d'extériorisation de vers adultes dans les selles et les vomissements ; les larves dans l’expectoration.
· diagnostic indirect : est inutilisable.
I.5.2.8. Traitement
· levamisole (Solaskil®, Decaris®): 50mg pour l’enfant ;
· albendazole (Zentel®) : cure de 400mg en une prise ;
· mébendazole (Vermox®) : cure de 600mg en 2 prises de 100mg pendant 3jours ;
· ivermectine( Mectizan®) distribution spéciale ; 150 μg par kg de poids.
Autre thérapeutique :
· Chirurgie en cas de complications.
Le suivi thérapeutique se fait par une coprologie 1 mois après le traitement.
I.5.2.9. Prophylaxie
· Prophylaxie générale :
La lutte contre le péril fécal, les mesures sanitaires et l’interdiction de l'épandage des engrais humains sont à mettre en application. L’utilisation des latrines.
Le traitement de masse doit être envisagé.
· Prophylaxie individuelle :
Elle est résumée à observer l’hygiène manuelle ainsi que le lavage des crudités.
I.5.3. Ankylostoma sp ou ankylostomes
I.5.3.1. Epidémiologie
C’est un parasite cosmopolite avec une prévalence élevée dans les régions humides et chaudes qui touche le 1/4 de la population mondiale. Elle est la 2è helminthiase après l’ascaris et est une maladie liée au péril fécal humain.
L’évolution larvaire est dépendante de la température (Ancylostoma T° >22 °C, Necator: T° >25 °C). C’est ainsi qu’il est retrouve dans les pays chauds et humides, dans les tropiques ou dans les zones à microclimat (mines, briqueteries).
N. americanuset A.duoudenale sont retrouvés en Afrique, en Asie et en Amérique.
Isolé, N. americanus prédomine en Amérique et en Australie. De même que A. duodenale, seul, prédomine au proche orient, en Afrique du Nord et au Sud de l'Europe.
I.5.3.2. Morphologie
· Adulte
Il a l’aspect de gros oxyures blancs (rouges après repas sanguin), possédant une capsule buccale inclinée sur la face dorsale et, il est hématophage.
Le mâle mesure 8-10 mm de long, il a une bourse caudale et 2 spicules permettant le diagnostic d'espèce.
La femelle mesure 10 -15 mm de long, son extrémité postérieure obtuse et une vulve au tiers postérieur qui prend la forme de Y.
Ancylostoma duodenale possède une bouche armée de 2 paires de crochets; la bourse caudale a une côte courte tridigitée.
Necator americanus possède une bouche armée d’une paire de lames coupantes ventrales et une paire de dents dorsales. La bourse caudale a une côte longue bidigitée.
· Œuf
Il est ovoïde et possède une coque mince, transparente, incolore avec à l’intérieur un embryon au stade 4, 8 ou 16 blastomères. Il mesure 57-76 µm sur 35-47 µm.
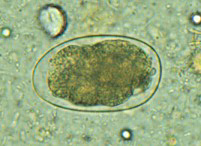
Figure 5.Œufd’Ankylostome (http: //www.dpd.cdc.gov/dpdx)
I.5.3.3. Habitat
Les adultes vivent dans le duodénum et jéjunum, attachés à la muqueuse par leur capsule buccale.
I.5.3.4. Cycle
Les œufs sont éliminés dans les selles et leur maturation s’accomplit lorsque la température est suffisante (25-30°C), en présence de l’oxygène et dans les conditions d’humidité. Cette cinétique est donnée à titre indicatif et dépend des conditions particulières.
· Le premier jour, l’œuf pondu est contenu dans les selles se trouvant sur le sol ;
· le 2ème jour, il y a éclosion de la larve L1 (rhabditoïde) libre ;
· le 3ème, la première mue s’effectue et il y a apparition de la larve L2 libre ;
· le 8ème jour, la larve L2 mue en larve L3 (filariforme ou strongyloïdes) qui reste dans l'exuvie de la mue, survie 1 à 2 mois (ou plus) dans les conditions environnementales favorables.
La larve L3 présente un géotropisme (tendance à monter, former des mèches), un histotropisme (attraction par la peau), un thermotropisme (attraction par la chaleur).
La contamination se fait par pénétration active transcutanée des larves filariformes L3 (réalisée en 5 minutes), accessoirement il y a possibilité d'ingestion (pour Ancylostoma uniquement).
Après leur pénétration par la peau, elles sont drainées par les veines au cœur jusqu’aux poumons. Elles percent la paroi de l’alvéole, remontent les bronches et la trachée, arrivent à la glotte où elles sont dégluties et se retrouvent dans l’intestin. Elles atteignent l’intestin grêle, où elles vont s’installer et devenir des vers adultes.
La majorité de vers adultes sont éliminés en 1 à 2 ans, mais leur longévité peut atteindre 5 ans.
Le fœtus peut être atteint in utero, et le nouveau-né par la lactation maternelle dans le cas d’A.duodenale.
En effet, certaines larves d’A. duodenale, après pénétration, peuvent devenir dormantes dans l’intestin ou le muscle (hypobiose). N. americanus, cependant, requiert une phase de migration transpulmonaire.

Figure 6. Cycle d’Ankylostome(http: //www.dpd.cdc.gov/dpdx)
I.5.3.5. Pathogénie
Les ankylostomes sont hématophages, et au moyen de deux paires de dents ventrales recourbées en crochets, les vers adultes mordent la muqueuse duodénale à laquelle ils sont fixés. La plaie causée par la morsure continue de saigner sous l’effet d’un produit anticoagulant sécrété par les vers. La spoliation sanguine journalière est estimée à 200 µl de sang pour A. duodenale comparativement à celle de Necatoramericanus qui est de 30 à 50 µl de sang.
I.5.3.6. Symptômes
· Phase d'incubation :
Elle correspond au passage transcutané des larves L3 qui se fait en 24 à 48 heures. Ce passage est accompagné de prurit, érythème papuleux, lésions de grattage (gourme des mineurs) et dure 6 à 8 jours.
· Phase d'invasion :
Elle correspond à la migration larvaire au niveau des poumons avec les signes suivants : toux afébrile, pharyngite, voix rauque (catarrhe des gourmes). Elle dure 1 à 2 semaines.
· Phase d'état :
C’est l’installation des vers dans le duodénum 6 à 8 semaines après la contamination.
Au 1ermois, on assiste à des manifestations telles qu’une duodénite avec des douleurs duodénales, nausées, vomissements, diarrhée, anorexie ou boulimie, perversion du goût, amaigrissement ; tout se normalise après 2 mois.
Lorsque l’infestation devient chronique, elle est caractérisée par des douleurs épigastriques. Après quelques années si l'infestation est importante et l'apport alimentaire insuffisant, il y a installation d’une anémie de type hypochrome, microcytaire, ferriprive ; généralement bien supportée.
L’intensité de l’anémie est liée à 3 facteurs : nombre et espèces des vers ; état de l’hôte (âge, sexe et état nutritionnel) ; durée de l’infection.
La spoliation sanguine due aux vers n'est pas compensée si le nombre est inférieur à 500 vers, mais chez la femme et l'enfant, les réserves en fer sont moindres et donc l'anémie peut se manifester si le nombre dépasse 50 vers. Des troubles généraux tels que l’asthénie, l’arrêt de croissance, les troubles nerveux peuvent également faire partie des symptômes.
En l'absence de réinfestation, la guérison intervient en 5 à 10 ans avec une restauration spontanée de l'anémie.
I.5.3.7. Stade diagnostic
C’est soit l’œuf avec une coque mince, unique et transparente; soit les larves rhabditoïde et filariforme.
I.5.3.8. Diagnostic
· Diagnostic d'orientation
ü séjour en région d'endémie ;
ü pendant la phase d'invasion : hyperleucocytose (12 à 20 000/µl = 12 à 20 G/L) et hyperéosinophilie (1500 à 10 000/µl = 1,5 à 10 G/L).
· Diagnostic direct
Il est possible à la phase d'état et est basée sur la coprologie différée en 24 heures. Au microscope, on observe les œufs (70 x 35 µm), embryonnés à l’émission. Un œuf dans une préparation standard (2 mg) représente 20 vers adultes.
Après 24 heures, on observe les larves L1 rhabditoïdes (250 µm) qui peuvent être confondues avec celles de S.stercoralisoude Trichostrongulyssp. Le diagnostic différentiel sera posé, sur la morphologie des L3, grâce à la coproculture parasitaire (Haradamori) pendant 7 jours à 28 °C et on aura les larves L3 strongyloïde engainée (600 µm).
I.5.3.9. Traitement
· levamisole (Solaskil®, Decaris®) : 50mg pour l’enfant ;
· albendazole (Zentel®) : cure de 400mg en une prise ;
· mébendazole (Vermox®) : cure de 600mg, en 2 prises de 100mg pendant 3jours.
Autre thérapeutique: fer, vitamine B12 en cas de forte anémie.
Le suivi thérapeutique doit être assuré par un contrôle parasitologie après 3 semaines, refaire après 9 à 12 mois en raison de l'hypobiose larvaire possible pour A. duodenale.
I.5.3.10. Prévention
· Prophylaxie générale
La lutte contre le péril fécal, l’éducation sanitaire, le dépistage et le traitement de masse annuel en région d'endémie.
· Prophylaxie individuelle
Le port des chaussures pour éviter le contact de la peau nue avec la terre.
I.5.4. Strongyloides stercoralis ou anguillule
I.5.4.1. Epidémiologie
Ce parasite est répandu dans les pays tropicaux et subtropicaux, mais aussi dans les pays tempérés.
Il est plus fréquent dans les milieux ruraux et les groupes socio-économiques pauvres.
I.5.4.2. Morphologie
· Adulte génération parasite :
Les femelles parthénogénétiques très fines, œsophage strongyloïde (à un seul renflement œsophagien), non hématophages, se nourrissent des tissus et mesurant 2,5 mm sur 0,04 mm.
· Œufs :
Ilssont proches de ceux des ancylostomidés, coque mince, claire, transparente, 50 x 30 µm et contiennent la larve L1 lors de l'émission des selles.
· Stades larvaires :
L1 : rhabditoïde (250 µm, double renflement œsophagien).
L2 : strongyloïde (500 µm, un renflement œsophagien).
L3 : strongyloïde infectieuse (600 µm, un renflement œsophagien, œsophage égal à la moitié du corps, l’extrémité postérieure discrètement bifide).
· Adultes de la génération stercorale :
Ce sont des adultes stercoraux d’environ 1 mm de longueur.
I.5.4.3. Habitat
Les femelles vivent enfouies dans les plis et la sous muqueuse des glandes de Lieberkûhn du duodénum et de l’intestin grêle.
I.5.4.4. Cycle
C’est le cycle le plus complexe avec alternation entre le cycle libre et parasitaire, le potentiel d’auto-infection et multiplication à l’intérieur de l’hôte.

Figure 7. Cycle de S.stercoralis(http : //www.dpd.cdc.gov/dpdx)
· Cycle libre :
Les larves rhabditoïdes éliminées dans les selles peuvent muer 3 fois et devenir larves infectantes filariformes (développement direct), ou muer 4 fois et devenir des adultes mâles et femelles libres qui vont s’accoupler et libérer des œufs d’où vont sortir des larves rhabditoïdes.
Ces dernières peuvent donner une nouvelle génération d’adultes libres ou des larves filariformes infectantes. Celles-ci pénètrent la peau de l’hôte humain pour un cycle parasitaire.
· Cycle Parasitaire :
Les larves filariformes se trouvant dans un sol contaminé pénètrent la peau humaine, et sont drainées par la circulation de retour jusqu’aux poumons via la veine porte, où elles traversent la paroi de l’alvéole, remontent les bronches et la trachée. Par la déglutition, ces larves arrivent au niveau de l’intestin grêle, et après 3 mues, elles deviennent de vers femelles adultes.
Ces dernières vivent enfouies dans la muqueuse du grêle et produisent par parthénogenèse des œufs qui vont libérer des larves rhabditoïdes.
Celles-ci peuvent être éliminées par les selles ou bien effectuer une auto-infection.
Lors de l’auto-infection, la larve rhabditoïde devient la larve filariforme infectante, et peut pénétrer la muqueuse intestinale (auto-infection interne) ou la peau péri anale (auto-infection externe). Elle peut dans ce cas suivre la voie décrite, en passant successivement dans les poumons, l’arbre bronchique, la glotte et l’intestin grêle où elles deviendront des adultes après une 4ème mue.
I.5.4.4. Symptômes
· Phase d'incubation :
Elle correspond au passage transcutané et en 24 à 48 heures, on assiste à un prurit, un érythème papuleux qui dure 2 à 3 jours.
· Phase d'invasion :
C’est la migration larvaire au niveau des poumons, accompagnée d’une toux afébrile, d’une pharyngite, d’une voix rauque (syndrome de Löffler). Cela se produit 4 à 6 jours après l'inoculation et dure 2 à 3 jours.
· Phase d'état :
Elle est caractérisée par l’installation des vers dans le duodénum, 20 à 30 jours après la contamination.
Les signes digestifs qui accompagnent sont les troubles du transit (diarrhées intermittentes ou chroniques, vomissements et nausées plus rarement).
On peut assister également à des troubles de la nutrition et à un amaigrissement (retard de croissance chez les enfants).
· Complications : neurologiques ou pulmonaires, sepsis chez les immunodéprimés.
I.5.4.5. Diagnostic
· Diagnostic d'orientation
ü Séjour en région d'endémie
ü Pendant la phase d'invasion : hyperéosinophilie (10 000 à 30 000/µl, 10 à 30 G/L), puis courbe en clocher ou en dents de scie.
· Diagnostic direct
Il est possible à la phase d'état.On peut réaliser une coproscopie et observer les larves L1 rhabditoïdes (250µm), mais les pontes sont faibles et irrégulières (20 à 50 œufs pondus /jour/femelle), d’où la technique de Baermann est nécessaire pour les concentrer.
· Diagnostic indirect
C’est la recherche facultative des anticorps sériques, mais l’interprétation est délicate en raison des réactions croisées avec d'autres nématodes et trématodes.
I.5.4.6. Stade diagnostique
C’est la larve rhabditoïde (250µm) qui possède une capsule buccale très peu profonde, une ébauche génitale très développée. Il peut aussi s’agir de la larve filariforme (500µm) qui est différente de celle d’ankylostomasppar un œsophage mesurant la moitié de la longueur totale, une extrémité postérieure fourchue et l’absence de l’enveloppe exuviale de L2.
5.4.7. Traitement
· ivermectine : une prise annuelle (distribution spéciale) ; 150 μg par kg
· thiabendazole (mintezol®): 50mg/Kg en dose unique après le repas ;
· albendazole (zentel®) : cure de 800mg, en 2 comprimés/j/3jours à répéter 3 semaines après ;
· mébendazole (vermox®) : cure de 600mg, en 2 prises de 100mg pendant 3jours.
· Chez le sujet immunodéprimé :
ü prolonger les cures de mintezol® pendant 6-7 jours et les répéter tous les mois pendant 6 mois ou alterner avec des cures d'ivermectine ;
ü suivi thérapeutique : faire des examens parasitologiques des selles à 1 mois, 6 mois et 1 an ; vérifier la chute du taux d'éosinophiles (remontée signifie rechute).
I.5.4.8. Prévention
· Prophylaxie générale
La lutte contre le péril fécal, l’éducation sanitaire, le dépistage et le traitement de masse annuel en région d'endémie.
· Prophylaxie individuelle
Le port des chaussures pour éviter le contact de la peau nue avec la terre.
· Prophylaxie pour les immunodéprimés
Chez les sujets ayant séjourné en pays d'endémie, faire la recherche d'anguillule avant tout traitement immunosuppresseur ou si risque de SIDA. Dans ce cas il y a sepsis à anguillules, qui sont isolées dans le sang car l’infestation est généralisée. Alors, l’anguillule est un indicateur de l’infection à VIH.
Même en cas de négativité, faire une cure de Mintezol® de 3 jours chaque mois à titre prophylactique.
Chapitre II : MATERIELS ET METHODES
II.1. NATURE ET PERIODE DE L’ETUDE
Notre étude est transversale, a été réalisée entre les mois de juillet et décembre 2017.
II.2.CADRE DE L’ETUDE
La rivière Kalamu est située dans la commune de Bumbu .Elle prend son origine non loin de l’hôpital général de Makala et descend vers Ngiringiri pour se jeter dans la rivière Ngunza dans la commune de Kalamu. L’étude est réalisée dans la commune de Bumbu.
II.3. POPULATION D’ETUDE
Notre population d’étude a été constituée des hommes et des femmes qui fréquentent la rivière et ceux qui habitent le long de la rivière. Une fiche élaboréereprenant les différentes variables nécessaires pour cette enquête a servi de collecter des données.
II.3.1. Critères d’inclusion :
· résider à BUMBU ;
· avoir au moins treize ans ;
· consentement éclairé de l’intéressé.
II.3.2. critères d’exclusion
Ce sont tous ceux qui ne répondent aux critères d’ inclusion
II.4. AUTRES MATERIELS
Les outils suivants ont constitué des matériels physiquesde la présente étude :
· Les fiches de collecte ;
· Les flacons ;
· Le formol ;
· Les échantillons des selles.
II.5. METHODE
II.5.1. Examen des selles après concentration (Ritchie modifié)
· Outils :
ü tubes a essaie,
ü les gaz hydrophiles,
ü les pipettes,
ü l’entonnoir,
ü le microscope,
ü les lames et lamelles.
· Réactifs
ü le formol ;
ü l’éther.
II.5.2.Principe
Les différents constituants des matières fécales gênant l’examen sont éliminés encours de préparation : les éléments protéiques sont coagulés par le formol, les graisses sont solubilisées par l’éther di éthylique. Les éléments figurés subsistent, la centrifugation les concentre dans le culot.
II.5.3 Procédure
Elle a consisté à :
· délayer les matières fécales dans une solution isotonique de formol à 10%
· filtrer à travers une double couche de gaze hydrophile dans un tube à centrifuger ;
· Ajouter de l’éther diéthylique à raison d’un volume sur dix, bien boucher le tube et agiter vigoureusement en maintenant le pouce,pour émulsionner le tout ;
· Centrifuger à 1500 tours par minutes pendant 3à 5 minutes ;
· Eliminer le liquide surnageant (couche supérieure d’éther diéthylique, couche supérieur de formol et anneau gras à l’interphase) ;
· Reprendre le culot et l’examiner pour la recherche des parasites au microscope à l’objectif 10X puis à l’objectif 40X.
II.6. ANALYSE STATISTIQUE
Dans la présente étude ; les données ont été saisies et analysées à l’aide du logiciel Microsoft Excel 2007. L’analyse et le regroupement étaient faits sous forme des pourcentages et des moyennes. Les données sont exprimées comme moyenne ± écart-type pour les paramètres métriques, et comme fréquences absolues ou relatives (en pourcentages) pour les paramètres catégories.
CHAPITRE III : RESULTATS
Notre étude est transversale, a été réalisée entre les mois de juillet et décembre 2017.Notre échantillon est constitué de 80 individus. Nos données seront représentées sous formes des tableaux et figures suivants :
III.1. Paramètres socio-démographiques :
La répartition de notre échantillon en tranche d’âge est reprise dans le tableau 1.
Tableau 1 : Répartition de cas selon les tranches d’âge.
|
Tranche d’âge (an) |
N |
% |
|
13 - 22 |
21 |
26,25 |
|
23 - 32 |
34 |
42,50 |
|
33 - 42 |
15 |
18,75 |
|
43 - 52 |
3 |
3,75 |
|
53 - 62 |
6 |
7,50 |
|
63 - 72 |
1 |
1,25 |
|
Total |
80 |
100,00 |
L’âge moyen a été de 30,03 ± 12,25 ans avec 13 et 65 ans comme extrême pour le plus de 5 ans. La tranche d’âge de 23 – 32 a constitué la classe modale.
Figure 8 : Répartition selon le sexe.

Le sexe masculin a été plus touché que le sexe féminin avec un sexe ratio de 4.
Tableau 2 : Répartition selon la profession.
|
Profession |
n |
% |
|
Chômeur |
30 |
37,5 |
|
Commerçant |
26 |
32,5 |
|
Elève |
19 |
23,8 |
|
Technicien |
3 |
3,8 |
|
Ménagère |
1 |
1,3 |
|
Etudiant |
1 |
1,3 |
|
Total |
80 |
100,0 |
La majoritaire de notre échantillon est constituée des chômeurs (37 ,5%) et commerçant (32,5%).
Tableau 3 : Répartition selon le lieu d’habitation.
|
LIEU D’HABITATION |
n |
% |
|
Tuwisana |
21 |
26,25 |
|
Lungueni |
12 |
15,00 |
|
Kisielele |
7 |
8,75 |
|
Luvambanu |
7 |
8,75 |
|
Zongo |
7 |
8,75 |
|
Landu |
6 |
7,50 |
|
Mabeka |
5 |
6,25 |
|
Masengi |
5 |
6,25 |
|
Souvenir |
5 |
6,25 |
|
Ngeba |
2 |
2,50 |
|
Luyindula |
1 |
1,25 |
|
Mpanzu |
1 |
1,25 |
|
Ndungini |
1 |
1,25 |
|
Total |
80 |
100% |
La plupart des personnes enquêtées réside sur l’avenue Tuwisana(26,25).
III.2. Prévalence des géohelminthes
Tableau 4 : Prévalence des parasites selon les résultats.
|
RESULTATS |
n |
% |
|
Positif |
55 |
68,75 |
|
Négatif |
25 |
31,25 |
|
Total |
80 |
100 |
La prévalence de géohelminthes est observée dans 68 ,75%.
Tableau 5 : Prévalence des géohelminthes selon les espèces.
|
RESULTATS |
n |
% |
|
Ascaris |
40 |
50,00 |
|
TrichurisTrichura |
20 |
25,00 |
|
A. duodénale |
5 |
6,25 |
|
Négatif |
25 |
31,25 |
Il ressort de ce tableau que l’Ascarislumbricoïdesa été retrouvé dans la moitié de l’échantillon soit 50 % des cas.
Tableau 6 : Répartition des autres parasites du tube digestif.
|
Espèce |
n |
% |
|
Kyste d’E.coli |
9 |
11,25 |
Hormis les géohelminthes le seul protozoaire rencontre est l’E. Coli.
Tableau 7 : Prévalence suivant le parasitisme.
|
Parasitisme |
N(80) |
% |
|
Monoparasitisme |
55 |
68,7 |
|
Biparasitisme |
15 |
18,7 |
|
Triparasitisme |
2 |
2,5 |
Le monoparasitisme a été le mode le plus fréquemment retrouvé (68,7%). L’association Ascaris lumbricoides-Trichuristrichura a été l’infection mixte la plus courante.
Chapitre IV : DISCUSSION
Dans notre étude réalisée dans la commune de Bumbu autour de la rivière de Kalamu, nous avions eu 80 échantillons. Faudra signaler que les nombreuses études existantes dans la littérature sont focalisées sur les enfants d’âge scolaire et préscolaire.
Pour ce qui est de la prévalence elle est de 68 ,7% différentes de celle de Menan et All (chez les enfants d’âge scolaire soit 36,46%) et Umesumbu (17,4% pour le moins de 5ans et 36,4% pour le plus de 5ans.La basse fréquence chez les enfants pourraient s’expliquer par l’existence des campagnes systématiques de déparasitage.
La tranche d’âge la plus affectée est celle de 23 à 32 ans différente de celle trouvée par Morenikeji 2009 située entre 0 à 29 ans. Cettedisparité serai due au fait que nous avons travaillé chez les adultes alors que Morendiji a travaillé dans la population générale.
Par rapport au sexe, le sexe masculin est significativement plus parasite que le féminin soit 80 % et un sexe ratio de 4 cela rejoignant l’étude de MENAN et all à Abidjan avec un sexe ratio de 1,2.ceci pourrait s’expliquer par le fait les activités attribuées aux deux sexes exposent le sexe masculin par rapport au féminin à un sol contaminé Notre étude ne correspond pas celle d’Umesumbu ou il n’existe aucune différence significative entre les deux sexe en République Démocratique du Congo.
Ascaris lumbricoides se place en tête des géohelminthes étudies dans 50 % suivi de Trichuristrichura (25%) Des résultats similaires ont été rapportés par des études menées dans plusieurs pays africains qui placent les deux premiers helminthes au premier rang. (Umesumbu et Mulumba).Cela est différent avec l’étude de Menan et all en Abidjan ou le Trichuristrichura vient en tête avec 23 % mais avec de prévalence proche de la nôtre parce que la trichocéphalose semblerait une pathologie urbaine en zone tropicale (OloODuntans et all).
L’ association avec les autres protozoaires étaientobservée dans cette étude soit l’existence des kystes d’Entamoeba Coli dans une proportion de 11,25%.La même observation a été faite dans le travail d’Umesumbu mais dans une proportion de 15,5%.Ces kystes confirment ainsi sa place du meilleur indicateur des mauvaises conditions hygiéniques confirmant ainsi la précarité de notre population d’étude.Les autres protozoaires pourront être vus dans cette enquête, hélas notre méthodologie de prélèvement et conservation dans le formol des selles et une analyse antérieure expliqueraient cette absence des protozoaires et même des formes trophozoïdes.
La coïnfection deAscaris lumbricoïdes et Trichuristrichura dans notre étude a été observées par d’autres publications aussi Congolaise qu’Africaine. Cette coïnfection n’a pas d’explication prouves scientifiquement si ce n’est des spéculations.
Chapitre V : CONCLUSION
Les géohelminthiases constituent un problème de santé publique vue la prévalence de notre étude soit 68 %.Elle constitue un problème non seulement des enfants d’âge scolaires et pré scolaires mais aussi des adultes constituant ainsi un réservoir souvent négligé. Les conditions géophysiques environnementales et l’hygiène défectueuse favorisent la pérennisation de ces pathologies négligées.
Les adultes sont infectes à de proportions élevées avec une prédominance de sexe masculin. Les coïnfections entres géohelminthes et a d’autres protozoaires intestinaux sont fréquentes.
Le taux sévères d’infestations signales sont lies à beaucoup des facteurs (l’ignorance des notions élémentaires l’humidité,marche pieds nus promiscuité…
Le déparasitage des enfants ne suffit pas à lui seul il faudra intégrer ces adultes surtout des milieux défavorisés.
RECOMMANDATIONS
1. Au Ministère de la Sante Publique : de promouvoir des actions concrètes en terme de salubrité et d’assainissement de l’environnement.
2. A la population :de respecter une hygiène rigoureuse en s’imprégnant des prescriptions élémentaires d’hygiène, notamment le lavage des mains avant de manger et après avoir été aux toilettes ,laver les fruits et autres aliments crus avant toute consommation ,assainir le milieu, encourager le port des chaussures.
3. Au personnel scientifique : de pencher des nombreux études des géohelminthes chez les adultes.
BIBLIOGRAPHIE
1. E.I.H Menan, N.G.FNebavi, T.A.K Adjetey, N. NAssavo, P.C Kiki-Barro et M.kone : Profil des helminthiases intestinales chez les enfants d’âge scolaire.
2. Rapport de l’OMS sur les maladies tropicales négligées publié en 2010
3. Rapport de l’OMS : aide-mémoire N° 366 Avril 2015 sur les géohelminthiases
4. Rapport de l’OMS :2014 N°13,133-140 : relevé épidémiologique hebdomadaire sur les géohelminthiases.
5. Série de rapport technique N°112 :schistosomiase et géohelminthiase. prévention et lutte,rapport d’un comité d’experts de l’OMS Genève(2002).
6. Dr NUNDU :Mémoire de fin de spécialisation sur les géohelminthiases.
7. Etude épidémiologique des helminthiases intestinales chez les enfants de la zone d’épandages des eaux usée.
8. OloOduntan S. The health of Nigerian children of school age (6-15 years). Ann. Trop Med Parasit1974 68, 145-156.
9. Morenikeji OA, Azubike NC, Ige OA: prevalence of intestinal and vecteur borne urinary parasites in communitris in south-west Nigeria. S.vector borne dis 2009.46:164-è.
10. Dr Umesumbu (Mémoire de spécialisation à Prévalence des géohelminthiases et facteurs de risques chez les enfants de Kinshasa.
ANNEXE
FICHE DE COLLECTE
1) Noms :
- Sexe :
- Age :
- Adresse :
- Profession
2) Usage de l’eau de rivière
Usage des WC Oui ‹ Non ‹
3) Présence ou non des toilettes Oui ‹ Non ‹
4) Type de toilettes
5) Lavage des mains avant de manger
Toujours ‹ Souvent ‹ Parfois ‹ Jamais ‹
- Lavage des mains après avoir été aux toilettes
Toujours ‹ Souvent ‹ Parfois ‹ Jamais ‹
Fréquentation de la rivière
Toujours ‹ Souvent ‹ Parfois ‹ Jamais ‹
Prurit/démangeaison
Douleurs abdominales
Diarrhée :
Sang cutanéo-muqueuse
Hépatosplénomégalie :
Amaigrissement
Laboratoire
Présence des œufs de schistosoma dans les selles
Oui ‹ Non ‹
 Vitrine de la RDC
Vitrine de la RDC


